预防I型糖尿病,从婴儿时期肠道菌群出发

文献导读
人肠道菌群会随着年龄、饮食,用药等因素变化而发生改变。目前,人类从出生到老年这一阶段的肠道菌群的动态变化仍缺乏清晰认识。婴儿期到儿童期这个时期被认为是人肠道菌群形成的关键阶段。此外,这一阶段的微生物和免疫之间的互作被认为是与后期多种疾病相关,特别是胰岛自身免疫(IA)或I型糖尿病(T1D)。
文献简介
- 英文标题: The human gut micro biome in early-onset type 1 diabetes from the TEDDY study
- 中文标题:最大规模研究揭示婴儿肠道微生物发展的三个阶段及对疾病的影响
- 作者: Tommi Vatanen (First Author), Curtis Huttenhower1,2,20* & ramnik J. Xavier (Corresponding Author) [专业领域:Computational and Integrative Biology]
- 单位:Broad Institute of MIT and Harvard, Cambridge, MA, USA.
- 期刊: Nature; 影响因子: 【40.137】Doi号: 10.1038/s41586-018-0620-2
文献摘要
目的:
I型糖尿病是因胰腺组织遭到免疫攻击而诱发的一种糖尿病,此前研究人员推测肠道菌群和糖尿病进展之间可能存在某种未知的关系,本文希望能够阐明机体胰腺功能或T1D和早期肠道菌群之间的潜在关联。
设计:
作者分析了10,913份来自于783名白人非西班牙裔儿童的肠道菌群样本数据。从出生后三个月开始每个月收集样本,直至The Environmental Determinants of Diabetes in the Young (TEDDY) 研究中的临床终点。
结果:
结果表明在对照组儿童肠道菌群中包含更多与发酵和短链脂肪酸(SCFA)生物合成相关的基因,但这些基因与地理上不同的临床中心的特定分类群并不一致,这表明与T1D相关的菌群在分类水平上是分散的,但在功能上更连贯。婴儿肠道菌群的分类水平和功能水平都是动态且高度个性化的,且在生命的第一年主要由三种双歧杆(B.bifidum,B.breve或B.longum)中的一种占主导地位或Proteobacteria门占主导地位。特别地,在母乳喂养的婴儿中存在用于利用人乳寡糖的基因的特异性菌株B.longum。
结论:
TEDDY分析提供了肠道菌群与胰岛自身免疫(IA),T1D和其他早期儿童发育事件相关详细的纵向功能谱。结合来自人群和T1D小鼠模型的现有证据,这些数据支持SCFA在早发性T1D中的保护作用。
背景介绍
在患有2型糖尿病(T2D)的成人肠道菌群中发现了产SCFA的细菌水平降低。此外,也有报道称IA后且T1D诊断之前,患者出现肠道通透性增加和微生物多样性降低。使用非肥胖糖尿病(NOD)小鼠模型的研究已经确定了SCFAs介导的保护作用和自身免疫中微生物组相关性别偏差的免疫机制。喂食特殊饮食的NOD小鼠增加SCFAs(醋酸盐和丁酸盐)的产量,使小鼠几乎完全免受T1D的影响。婴儿与成人的肠道菌群特征明显不同,微生物组成差异显著,有氧呼吸在能量代谢中的比例更大,动态变化更为极端。这些差异在生命的最初几年会逐渐消失,特别是固体食物的引入。个体微生物菌群发育轨迹受环境,分娩方式,母乳(配方)喂养和抗生素的影响。大多数针对肠道菌群与T1D相关的研究都是使用了16S的数据,但16S的数据不易检测到的功能和菌株特异性差异而难以解析疾病的发病机制。
技术路线图
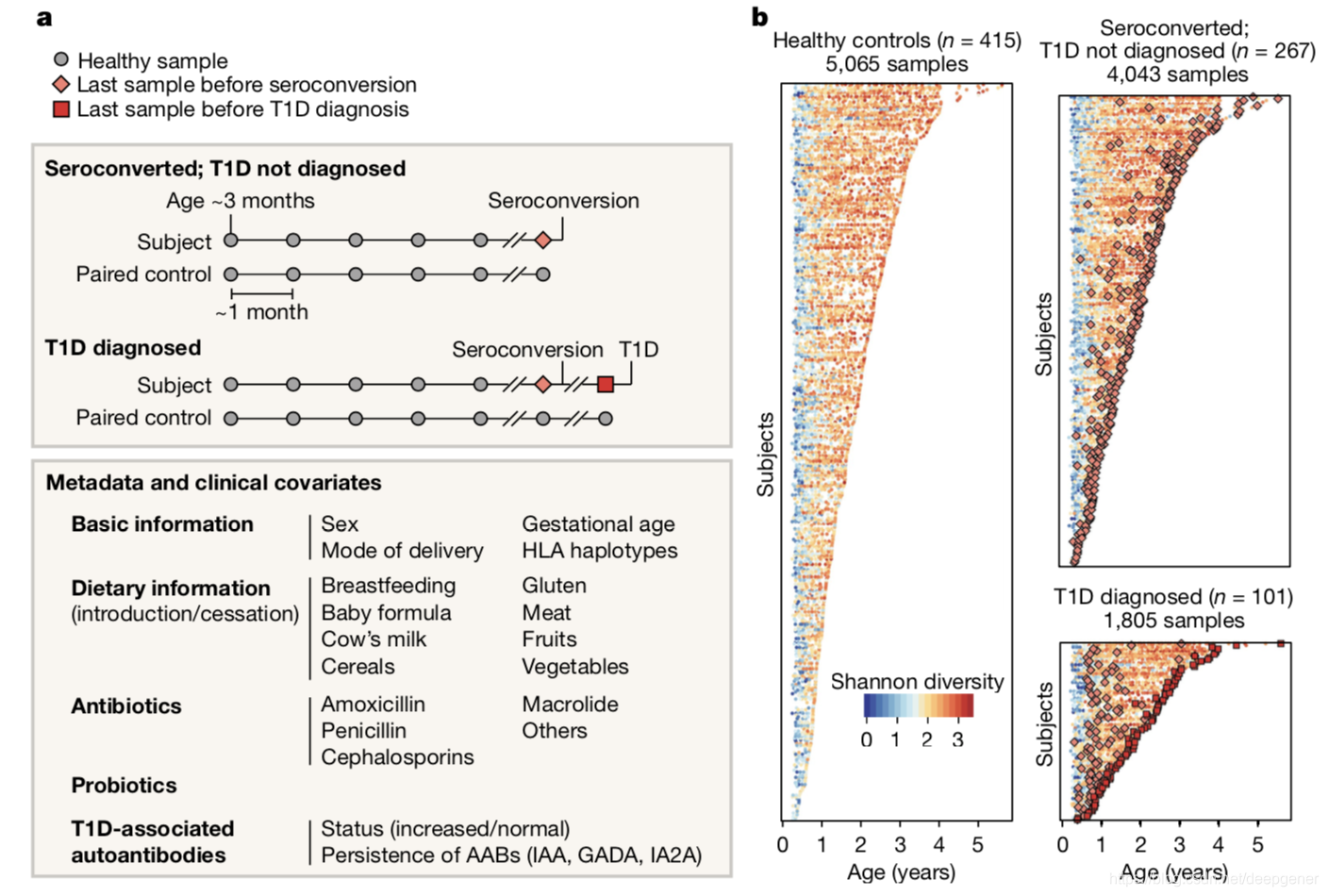
结果
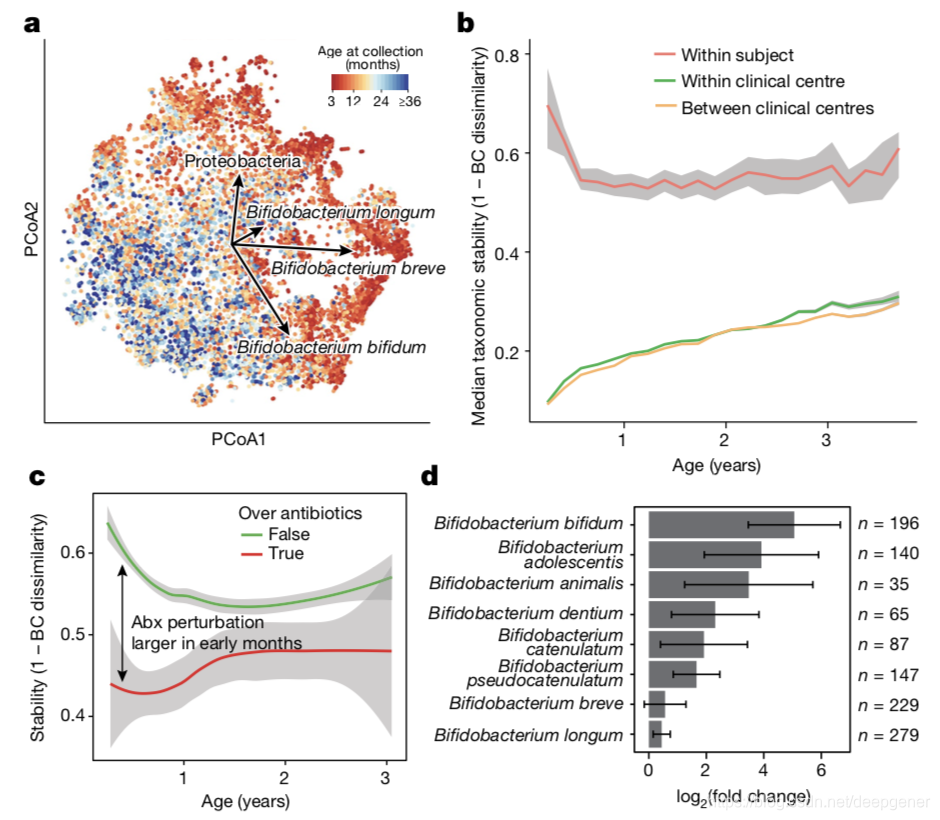
基于Bray-Curtis距离的beta多样性结果显示最早期样本展示了非常强的纵向梯度和显著的异质性,受试者之间的差异解释了35%的肠道菌群组成变异,其次取样时的年龄约解释4%方差。作者发现除了受试者ID和年龄,地理位置和母乳喂养对肠道菌群的组成具有显著影响,母乳喂养的停止对早期生活肠道菌群α多样性具有最大的影响。口服抗生素的过程破坏了肠道菌群稳定性,且在最早期的效应最大。服用抗生素后,某些双歧杆菌含量会下降,而B.longum和B.breve没有系统地下降(图2d),表明某些双歧杆菌物种在抗生素耗尽后特别容易受到其他群落成员的竞争。鉴于它们在肠道菌群中的主导地位以及与母乳代谢相互作用的微调平衡,这一发现强调了在儿童早期接受抗生素处方的重要性,特别是在母乳喂养期间。
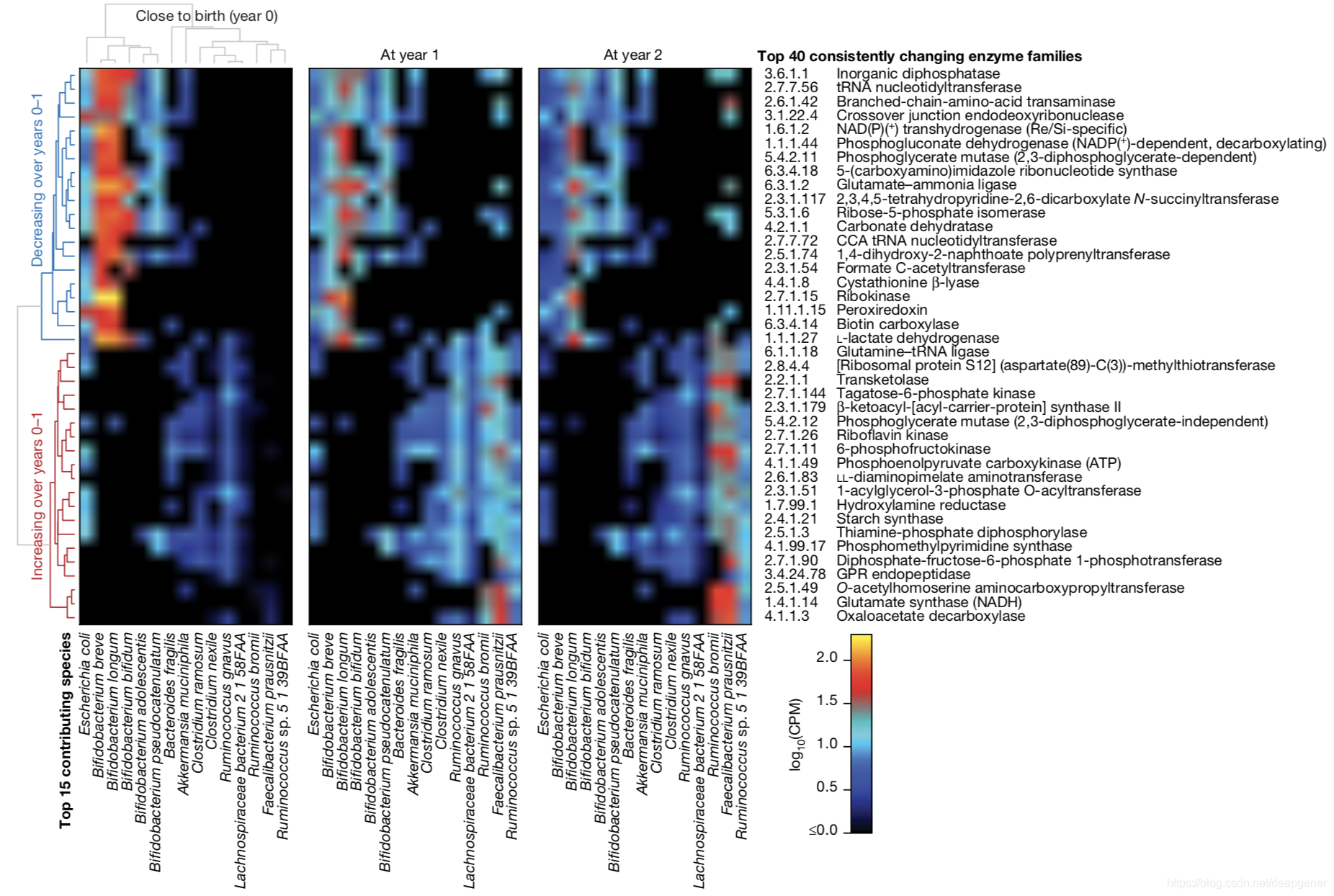
除了广泛保守和特定的功能外,有一系列微生物代谢酶在生命的第一年中持续增加或减少,这与肠道菌结构和婴儿饮食的变化相似。这些显著变化突出了早期婴儿肠道的独特代谢环境,随后转变为更适合于发酵产能的成人的肠道菌群。在IA患病组和对照组群体中,对照组含有较高的Lactobacillus.rhamnosus菌,这说明可以通过早期益生菌补充来降低IA的风险。同时,对照组还具有更多的双歧杆菌,而IA患病组具有更高的链球菌。在T1D病例对照比较中,对照组的嗜热链球菌和乳酸乳球菌。与发酵相关的超级途径在T1D和芬兰IA的对照组中显著富集,几种促成SCFA生物合成的细菌途径增加。具有益生菌和益生元功能的母乳是决定婴儿肠道菌群组成的主要因素之一。在母乳喂养期间,总共观察到41个更富集的基因家族,大多数由B.longum菌携带(图4)。在含有B.longum菌的样品中,当较少的B.longum菌菌株携带这些基因时这意味着断奶后发生明显的菌株转变。

讨论
确定个体间肠道菌群与T1D发病机制之间关系对未来靶向疗法是有益的,特别是考虑本文揭示的明显群体水平异质性。不同的内源性疾病,自身抗体(IAA与GADA)的差异,自身抗体的数量,从血清转化到T1D诊断的时间,遗传宿主高风险等位基因和种族背景,可能都会导致具有不同的微生物特征。通过横断面数据和更详细的纵向调查,该研究为进一步鉴定T1D风险或发病机制中具有预测性,保护性或潜在因果关系的肠道菌群奠定了基础。
思考
尽管样本量充足,对研究设计进行了详细审查,并进行了全面的统计分析,在case-control比较中检测到的大多数分类水平和功能信号通路的效果大小和统计学意义都不大。这是由于几个原因如T1D的endotype,时间弥散信号,地理异质性或生命最初两个月粪便样本的缺乏等导致的差异。此外,这些研究中使用的数据包括来自遗传易感性和大多数白人非西班牙裔case-control的样本,这些样本被设计到TEDDY研究中,不能保证结果能反映各个国家的整个TEDDY队列或儿童人群。
前景应用
文章详细阐述了婴儿肠道菌群的形成,深度剖析了微生物组、婴儿发育以及I型糖尿病之间的潜在关系,为将来靶向治疗夯实基础。
参考链接
深度基因小伙伴温馨提示:
-
如果我们对文章理解有偏差,非常欢迎大家向我们反馈,我们会认真阅读建议并修改,另外有意愿加入我们的小团队的老师和同学可发送邮件至我们的邮箱:[email protected] 祝大家科研顺利,生活开心!
-
想要了解更多内容请访问我们的深度基因网站:http://deepgener.wordpress.com/
-
点击查看上一篇文献内容