摘要:
综述类文章怎么写
背景
在摩尔定律的推动下,各类电子产品更新迭代,推陈出新,以满足人们对于消费电子日益增长的需求,同时这也产生了大量废弃的电子产品。现如今的电子产品通常是用不可分解的,非生物相容性的,有时甚至是有毒的材料,导致世界范围内严重的生态挑战。此外,电子产品的生产制备过程中消耗了大量的比如镓铟等稀缺元素(铟镓锌氧化物已广泛用于许多薄膜晶体管中,例如有源矩阵有机发光二极管背板,射频识别标签和传感器设备等【1】),他们被淘汰和丢弃后很难重复利用,因此不利于地球和资源的可持续发展。
综上所述,开发可降解,生物相容的“绿色”电子产品,作为一个新兴课题受到越来越多人的关注。此类设备由可生物降解的材料制成,在环境或生理条件下以可控的速率起作用后,可以完全或部分溶解,吸收或物理消失,因此又被称为“瞬态电子设备”或“可生物降解电子设备”。
这类设备不仅仅是环境友好,资源节约的,还因其可生物降解的特性可以被应用于很多场合:(1)用作人体植入医疗器件,比如可生物降解的缝合线或心血管支架,从而省去了进行第二次外科手术以进行设备修复的机会,并降低了相关的感染风险。(2)制备能够自我破坏并保护信息免受未经授权的访问的瞬态设备可以用作数据安全硬件,消除了回收操作产生的相关成本和风险。
related work
- 研究历史(时间轴讲)
- 目前的几种手段(按照分类讲)
- 尚且存在的问题(每一种技术是什么,可以参考摘要的总结)
- 目前对有机电子器件的研究大多集中在材料的合成和器件的制造,但很少关注它对环境的影响和器件相容性。
- 尽管已经研究了一些可生物降解的小分子,例如β-胡萝卜素和靛蓝衍生物(12,13),但这些小分子半导体的载流子迁移率很低(<0.1 cm2/ Vs)或需要高真空沉积工艺。
瞬态器件的可降解性是因为采用了生物可降解的材料,比如天然或合成的可生物降解的聚合物,这类材料主要由基质成分【2】实现,可以在生物医学或环境应用的水溶液中发生降解。
迄今为止,已证明的瞬态器件主要与针对生物医学或环境应用的水溶液降解有关[1e4,10]。研究人员已经对瞬态电子的生物可降解材料进行了研究,包括材料溶解化学,降解建模,制造技术,设备集成等。早期的尝试一直集中在有机材料上,包括天然或合成的可生物降解的聚合物,部分可降解的设备已经被开发出来。主要由基质成分[11e13]实现。最近的研究表明,单晶硅纳米膜(mono-Si NMs)在生理环境中的溶解速度为每天几纳米到100 nm以上[1,2,14,15],具体取决于类型水溶液。可分解的硅纳米管与可降解的无机电介质,金属和聚合物基材一起,可实现具有出色操作特性的完全可生物降解的电子产品,这些特性也可与半导体铸造工艺兼容[16,17]。已经开发出新颖的制造技术,以使可生物降解材料的敏感特性适应设备集成,防止材料被溶剂,温度或水破坏。在生理溶液中已证明了多种完全可生物降解的设备,包括热疗设备[1],颅内压传感器(ICP)[18],皮质醇(ECoG)记录系统[19],射频(RF)电子设备[ 20],电池[21],药物输送系统[22]等。为了在一定时间段内实现稳定的运行,并在随后的瞬态中实现过渡,封装材料至关重要。所获得的瞬态器件的功能寿命主要由封装材料的降解时间和透水性以及有源电子元件的厚度决定。外部触发刺激(水分,温度,光线,机械力等)是确定瞬变起点的替代因素,并且在非水环境中显示的触发降解主要与非生物应用有关。在这些情况下,设备可以完全瞬态或部分降级。
真菌降解的纤维素-纳米纤维纸制备的器件【3】
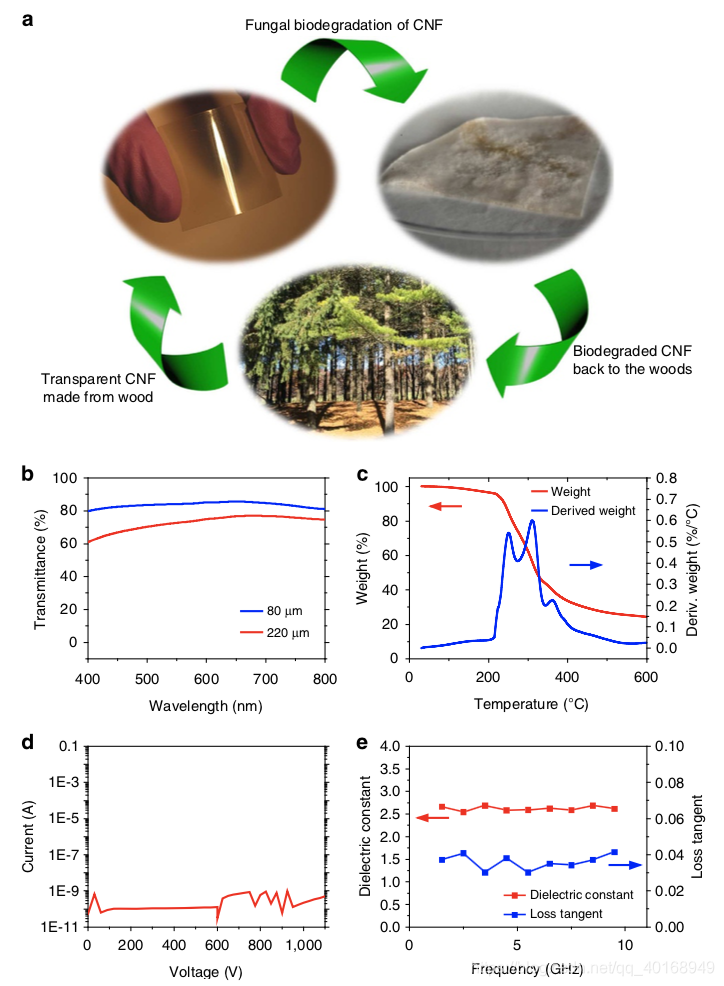
图注:介绍了纤维素-纳米纤维(CNF)纸及其作为电子衬底的基本特性。(a)以生物为基础和可降解的CNF纸生命周期的说明。首先,从木材中提取纤维素纳米纤维(CNFs)制成CNF纸。CNF纸可以通过真菌生物降解被降解并送回森林,而不会对环境产生不利影响。(b)可见光光谱上的透过率曲线。蓝色和红色曲线分别表示80毫米和200毫米厚的CNF薄膜的透光率。©热重(TGA)图,显示CNF膜的重量随温度的变化,以及曲线的一阶导数。薄膜在213°C时保持稳定。(d) CNF膜的电击穿特性。电流是在薄膜两边加高压时测量的。(e) CNF薄膜的射频特性。介电常数(红色)和损耗正切(蓝色)是使用微带波导在0到10ghz的频率范围内测量的。
【3】High-performance green flexible electronics based on biodegradable cellulose nanofibril paper
【4】Biocompatible and totally disintegrable semiconducting polymer for ultrathin an ultralight
weight transient electronics
共轭聚合物可以在机械上具有柔性、可拉伸性,并可在低温下进行溶解处理,这使得它们能够适应低成本的柔性和可拉伸电子产品的卷对卷制造(14)。最近对施主-受体(D−A)聚合物的开发极大地改善了器件的性能,场效应晶体管(FET)的规模超过了非晶硅(0.1−1 cm2/Vs),太阳能电池的效率超过了10%(15,16)。共轭聚合物已经成为柔性TFTs最有前途的候选材料之一。与非共轭可分解聚合物相比,共轭可分解聚合物的分子设计选择非常有限,因为可分解的分子构建块很少。据我们所知,目前还没有关于完全可分解的共轭多聚体或聚合物电子器件的报道。
为了实现零足迹的“绿色”电子产品,一种理想的方法是使用半导体聚合物,这种聚合物可以从自然资源中合成并分解回环境中(图1A)。在这项工作中,我们演示了图1A中“理想循环”的几个关键步骤,使用亚胺键作为可逆共轭连接剂来举例说明一种完全可分解的共轭聚合物及其在有机电子学中的应用。超薄电子产品提供了超轻量、超常的灵活性和更好的一致性,这对微细电子产品(7)、保形生物传感器(17)和可拉伸设备(18)都很重要。虽然在塑料基板上的超薄和轻质有机柔性器件,如聚对苯二甲酸乙二醇酯(PET),已经被开发(7,18,19),我们在这里报告一种基于纤维素的用于超轻量(2g /m2)电子器件的可生物降解超薄(800纳米)基板(图1B)。我们的衬底在各种常用的有机和水溶液中稳定,并且高温稳定(玻璃化转变温度(Tg) >180°C),因此与电子制造工艺高度兼容。利用这些材料,我们着手制造超薄柔性伪互补金属氧化物半导体(CMOS) cir- cuits具有高增益和轨对轨输出电压摆动在低工作电压4v。使用铁电极,我们展示了完全可分解的瞬态器件,我们观察了这些器件在轻度酸性条件下30天后的完全分解。
【1】Fully Bioabsorbable Natural-Materials-Based Triboelectric Nanogenerators
不断增长的神经系统疾病和心血管疾病要求创新和开发可植入医疗设备(IMD)。[1-4]这些设备主要包括传感器,胃和心脏起搏器,心脏复律除颤器以及深部脑,神经刺激器。 [5-7]长期的体内诊断和治疗对IMDs组件的高可靠性,良好的生物相容性,最小的毒性和微型化提出了很高的要求。现有大多数IMD的电源都依靠可充电或不可充电电池。[8-10]但是,内部发热量,容量损失和电池故障是此类电源的常见问题。这些电池完成任务后,患者必须进行第二次手术以将其取出,并承担相当大的经济负担以及严重的疼痛。因此,迫切需要开发一种新的方法来绕过这些障碍并避免长期植入后发生感染和发炎的风险。
最近,提出了摩擦电纳米发电机(TENG),并已证明可以有效地将环境机械能转换为电能。[17-20]转换机理取决于摩擦电效应与静电感应之间的耦合。这项新兴技术为无电池电子设备提供了替代解决方案。先前的研究表明,TENG在转换生物机械能方面具有卓越的性能,例如心跳,呼吸运动,肢体运动和脉搏搏动。[21–26]转换后的电能在心脏起搏器,健康监测,细胞和组织工程中得到了成功。 [26–31] Zheng等。在2016年首次报道了可生物降解的TENG包括人造合成聚合物(聚(乳酸-乙醇酸共聚物)(PLGA),聚(3-羟基丁酸酯-co-3-羟基戊酸酯)(PHBV)和聚己内酯(PCL)),[31]从公司购买。但是,这些市售聚合物通常价格昂贵,并且含有潜在有害的化学物质。与这些合成聚合物相比,天然聚合物因其低成本,易得性,可更新性和良好的生物相容性而受到越来越多的关注。[32-35]这些特性使其在生物医学领域具有广泛的应用,例如药物输送,可吸收缝合线[36-41]这些天然生物可吸收聚合物(NBP)主要包括纤维素,甲壳质,丝素蛋白(SF),宣纸(RP),蛋清(EW)等。这些材料具有出色的生物降解性,易加工性和良好的成膜性,从而使其适合用于体内TENG组件。
在此,利用上述天然生物可降解材料,开发了各种完全生物可吸收的天然材料基础TENGs (BN-TENGs)。与先前报道的TENGs相比,[31-35]这项工作首先使用五种天然材料在体内完全可吸收的BN-TENGs。首次通过成对组合试验对这些材料的“摩擦电系列”进行了综合研究,极大地推动了天然材料在滕钢等摩擦电器件中的应用发展。通过蚕丝蛋白膜的包封,将BN-TENG的体内外操作时间由几天调整为几周。利用所提出的BN-TENG作为电压源来驱动体外电刺激系统,成功地调节了分离的功能失调心肌细胞簇的功能。心肌细胞簇的搏动速度加快,收缩一致性增强。BN-TENG对功能性障碍心肌细胞的治疗效果为治疗某些心脏疾病如心动过缓、心律失常提供了一种新的、有效的解决方案。在SD大鼠中,BN-TENG完成其功能后可以被完全降解和再吸收。本发明具有可操控性、生物吸收性、低成本、易获得性等优点,在未来瞬态电子和集成电路领域具有巨大的应用潜力。
在此,利用上述天然生物可降解材料,开发了各种完全生物可吸收的天然材料基础TENGs (BN-TENGs)。与先前报道的TENGs相比,[31-35]这项工作首先使用五种天然材料在体内完全可吸收的BN-TENGs。首次通过成对组合试验对这些材料的“摩擦电系列”进行了综合研究,极大地推动了天然材料在滕钢等摩擦电器件中的应用发展。通过蚕丝蛋白膜的包封,将BN-TENG的体内外操作时间由几天调整为几周。利用所提出的BN-TENG作为电压源来驱动体外电刺激系统,成功地调节了分离的功能失调心肌细胞簇的功能。心肌细胞簇的搏动速度加快,收缩一致性增强。BN-TENG对功能性障碍心肌细胞的治疗效果为治疗某些心脏疾病如心动过缓、心律失常提供了一种新的、有效的解决方案。在SD大鼠中,BN-TENG完成其功能后可以被完全降解和再吸收。本发明具有可操控性、生物吸收性、低成本、易获得性等优点,在未来瞬态电子和集成电路领域具有巨大的应用潜力。
如图1a所示,BN-TENGs的所有聚合物成分均来自自然界,包括纤维素,甲壳质,RP,SF和EW。纤维素可以由木材和棉花制成。甲壳质可以从蟹壳和虾壳中提取; RP通常来自小麦,玉米和大米。 EW和SF可以分别从卵和茧中收集。所制备的BN-TENG由NBP和具有垂直接触分离模式的镁(Mg)电极组成(图1b)。来自几丁质,纤维素,SF,RP和EW的任何两个不同的NBP(NBP1和NBP2)都可以充当摩擦层,而超薄的Mg膜则可以用作背电极。用感应耦合等离子体反应离子蚀刻(ICP)处理NBP的摩擦表面,以形成纳米结构阵列,以扩大有效接触面积并增强接触带电。所获得的纳米结构阵列致密且均匀,平均高度约为100 nm(图1c,d)。在摩擦层之间放置了两个NBP垫片,以有效地将它们分开。 SF膜用作封装层,以保护BN-TENG免受外部环境的影响(图1b)。
例如,当我们选择SF和RP作为摩擦层时,制造的BN-TENG的最大输出电压和电流值分别为34 V和0.32μA(图1e,f)。当测量仪器反向连接到BN-TENG时,输出电压和电流信号相应地反转,这表明信号是由BN-TENG产生的(图1g,h)。 BN-TENG的有效输出功率通过监视电压和电流来评估,电压和电流的可变负载电阻范围为1kΩ至1GΩ(图1i)。由于欧姆损耗,电流幅度随负载电阻的增加而减小,而电压遵循相反的趋势,在负载电阻约为67MΩ的情况下,可实现21.6 mW m-2的最佳功率密度(图1j)。图1j中的插图表明,BN-TENG可以立即点亮十个商用绿色LED。这些LED通过在不使用外部电源的情况下按下并释放BN-TENG来直接供电。结果表明,预制的BN-TENG可以有效地将周围的机械能转换为电能,并为其他电子设备供电。
生物相容性是植入式设备的基本要求之一,而植入式设备在很大程度上取决于封装策略和组件材料。在本文中,将五个NBP加工成薄膜,并通过L929细胞评估其生物相容性。将这些NBP制备成尺寸为1cm×2cm,厚度为100μm的薄膜,这显示出优异的成膜能力。所有这些胶片都具有一定程度的透明度和柔韧性(图2a和图S1,支持信息)。 NBP膜的相对粗糙的表面也促进了细胞在其表面上的附着和增殖(图S2,支持信息)。通过3-(4,5-二甲基噻唑-2-基)-2-溴化2,5-二苯基四唑(MTT)分析研究了L929细胞在五张膜上的生存能力(图2b)。将对照组1、2和3 d的光密度值设为1,并选择其作为其他相应实验组的参考值。孵育1 d后,L929细胞在五张膜上的相对生存力均高于95%。接种2 d和3 d后,L929细胞在5张膜上的相对生存力均高于96%。统计结果也显示在图2b中。这些结果表明,在这些膜上培养的L929细胞可以生长和增殖而没有明显的停滞,这证明这五个NBP本质上无毒。
一步研究L929细胞在这些NBP膜上的附着,增殖和形态,分别在第1、2和3 d进行了免疫荧光染色(图2c)。培养24小时后,低密度的L929细胞表现出良好的附着力和细胞形态,就像单细胞一样(图2c中1d)。孵育2天和3天后,L929细胞明显达到高细胞密度,并显示出良好的丝状,拉伸形态(图2c中的2天和3天)。出现了一些细胞簇,甚至形成了融合的细胞单层(图2c中的3 d)。结果与MTT分析一致,表明L929细胞在这些膜上显示出良好的附着,扩散和生长。这表明五个NBP具有生物相容性且无毒,可以保证植入的BN-TENG的生物安全性。
预制的BN-TENG(图S3和S4,支持信息)通过接触和分离模式将机械能转化为电能。摩擦层之间的摩擦电效应和静电感应的耦合在两个反电极之间产生电子的交替流动。[42,43]如图3a所示,当外力使摩擦层与顶部之间发生物理接触时在底面和底面,分别为NBP的不同电子亲和力创建了带相反电荷的表面(图3a中原始图和压制图)。一旦外力消失,
摩擦层被垫片隔开,后电极之间的电位降推动自由电子从一个电极转移到另一个电极,以平衡静电场(图3a中释放)。当间隙从最小增加到最大时,由摩擦带电引起的电位降逐渐消失(在图3a中释放)。当外力使摩擦层再次接触时,感应的电子将回流并产生反向电流(图3a中的压力)。摩擦层的周期性接触和分离导致外部电路中产生AC输出信号。
在图3 b。电子束和卡普顿的结对显示最大转移电荷(12 nC), RP和卡普顿的结对显示最小转移电荷(5.5 nC)。根据转移电荷的不同,五层薄膜的摩擦电级数定义了一种新的>SF>几丁质>纤维素> RP从正到负(图3b)。在此基础上组装了各种BN-TENGs。不同的两两组合,纯属捏造BN-TENG实现广泛的可调输出性能Voc从8到55从0.08到0.6 V和IscμA(图3 c和图S5,支持信息)。低电流可以归因于BN-TENG的体积小(1 cm×2 cm)和直线电机的低跳动频率。[46,47]这些结果表明,BN-TENG可以满足广泛的电力输出需求,例如不同的生物电刺激电压或为不同的能耗设备供电。
据此前报道,甲醇可以改变分子结构的科幻小说从随机线圈β-sheet共同形成,这有助于加强BN-TENG的抗磷酸缓冲盐(PBS)和体液。[48-50]为了使BN-TENG在SD大鼠中达到可控的操作时间,分别制备了未经处理的SF (U-SF)和经甲醇处理的SF (M-SF)膜作为BN- tengs的包封层(图S6,支撑信息)。分别在体外(图4a,c)和体内(图4b,d)研究了BN-TENGs的生物降解性和生物吸收性。
如图4a,c所示,U-SF和M-SF膜包裹的BN- tengs在PBS中1 d时结构完整。7 d后,U-SF膜包裹的BN-TENG整体结构因聚合物骨架断裂而发生膨胀和起皱。Mg电极因水渗入被PBS完全腐蚀。21 d后,约四分之一的BN-TENG由于结构开裂而消失。当BN-TENG在PBS中浸泡较长时间后,自催化水解和本体降解迅速发生(42 d),并且初始结构降解并溶解在PBS中(84 d)。这些结果表明,M-SF膜可以显著保护BN- TENG不被水解,并抑制其在PBS中的降解。
如图4b,d所示,在体内,U-SF和M-SF包封的BN-TENGs都在1天时保持结构完整性。 U-SF封装的BN-TENG在聚合物骨架的骨架下膨胀并起皱。 7 d在BN-TENG的边缘形成一些缝隙。 21 d后,体内包裹了U-SF的BN-TENG被分解为两个部分,这可归因于SD大鼠的代谢,BN-TENG周围的纤维组织和组织的代谢。 SD鼠本身的日常运行。 42和84 d后,BN-TENG的裂纹部分降解并被SD大鼠吸收。相比之下,M-SF封装的BN-TENG在体内的降解速度要慢得多。它保持结构完整性直到42 d。直到84 d形成了明显的形变,表明M-SF膜还可以有效地减慢BN-TENG的体内降解速度。以上所有结果证明BN-TENG在体内和体外具有良好的生物降解性。通过修饰SF包封层,可以有效地控制BN-TENG在体外和体内的降解速率,这为设计用于短期和长期应用的可植入BN-TENG提供了指导。此外,考虑到将来的实际应用,可以通过选择新材料,结构设计或化学/物理改性来增强BN-TENG对生物环境的抵抗力,从而进一步提高整个设备的灵活性和耐用性。
为了证明所制造的BN-TENG能够将生物机械能转化为活体中的电能,将包裹有U-SF和M-SF膜的BN-TENG(SF / RP)植入SD的皮下背部区域大鼠(图5a和图S7,支持信息)。所有植入操作均严格按照“北京市实验动物管理规定”和国家标准“环境和住房设施的实验动物要求(GB 14925-2001)”进行。植入后立即缝合伤口。 8周后,伤口愈合良好,未见明显感染和炎症。体内电输出性能
在不同的时间测量BN-TENG。如图5b-d所示,将M-SF封装的BN-TENG植入SD大鼠的背部皮下区域。将SD大鼠在13周后进行安乐死,将其在植入部位含有残留BN-TENG的皮下组织用于组织学研究。苏木精和曙红(H&E)染色的组织切片显示,BN-TENG的一些残留物(蓝色箭头)存在于皮下层和肌肉层之间(图5e)。残留物被少量的纤维组织和巨噬细胞所包围。在残基之间的间隙中形成了一些含有巨噬细胞的再生正常组织(绿色箭头)。没有观察到嗜中性粒细胞和明显的炎症,表明BN-TENG具有良好的体内生物相容性和生物吸收性。
在整个体内植入过程中都记录了BN-TENG的电输出(图5f,h,i)。对于M-SF封装的BN-TENG,在11 d时输出电压从4.5 V降至1.2V。这可以归因于BN-TENG周围纤维囊周围的约束,包封层的起皱皱纹和摩擦层的机械性能下降(图5f,h)。尽管溶胀的包封层会限制BN-TENG的接触和分离,但在摩擦层之间不会发生体液渗透。 BN-TENG的输出性能随植入时间的延长而减弱。 4周后,电极线从Mg背面电极脱落,表明体液已经渗透到Mg的包封层中并且腐蚀了Mg背面电极。与U-SF薄膜相比,M-SF薄膜不仅可以保持良好的结构完整性,而且可以在较长的时间内保持较慢的质量损失(图5g)。此功能使M-SF封装的BN-TENG可以长期运行。
还用短期操作时间评估了U-SF封装的BN-TENG的电输出性能(图5f,i)。与M-SF封装的BN-TENG相比,U-SF封装的BN-TENG表现出快速的降解行为。体内输出电压在24小时内从3 V迅速下降到0.6 V(图5f,i)。 72小时后,体内电子输出被完全破坏。原因可能是由于包封层的水解,BN-TENG的摩擦电效应由于体液渗透而受损。体外生物降解测试还显示,U-SF包封的BN-TENG的质量快速下降(图5g)。由于U-SF层和Mg电极的快速溶解和水解,在7 d时仅保留了初始质量的37.5%。这导致在短时间内破坏了BN-TENG的结构完整性并造成了明显的电输出损耗。
以上结果表明,BN-TENG具有良好的生物相容性和生物吸收性。预制的BN-TENG可以在可控制的操作时间内将生物机械能有效地转化为体内的电能。通过修改SF封装层的长期和短期应用,可以有效地调节BN-TENG的工作时间。完成工作后,BN-TENG可以被SD大鼠降解并吸收。
组织工程学中的电刺激为细胞调节和组织修复提供了理想的途径。各种研究证明了其在临床和研究环境中的可行性和有效性。[51–53]这里,BN-TENG的电输出具有相对较高的电压和较低的电流,这有利于在生物医学领域进行电刺激。为了证明利用BN-TENG调节心肌细胞团跳动的实用性,将制成的BN-TENG和叉指电极集成到自供电刺激系统中。如图6a所示,刺激系统由BN-TENG,整流器和微间隙叉指电极组成。叉指式电极包装有50μm厚的聚二甲基硅氧烷(PDMS)薄膜,以避免电极与培养基之间发生电化学反应(图6c)。由BN-TENG产生的18 V整流输出电压连接至叉指电极以形成DC电场(图6a,b)。考虑到PDMS封装层的厚度,心肌细胞和设备之间的界面处的实际电场(EF)强度约为8 V cm-1,这是通过有限元模拟计算得出的(图S8,支持信息)。
然后将原代心肌细胞播种到叉指电极的表面。根据以前的报道,心肌细胞可以通过介导细胞间通讯的间隙连接蛋白(即连接蛋白)产生电互连。[49-52]在孵育过程中,接种的心肌细胞相互连接,形成了孤立的心肌细胞簇在电极间隙(图6d)。孵育48小时后,在电刺激之前,心肌细胞簇(图6d中的C1,C2,C3和C4)缓慢停顿(视频S1,支持信息),并出现了长时间的停顿。簇中的心肌细胞收缩微弱且无活性,尤其是C2和C3中的心肌细胞。然后,用来自BN-TENG的DC-EF在1 Hz下连续刺激心肌细胞簇30分钟。
用BN-TENG电刺激后,四个心肌细胞簇的跳动速度显着加快。簇中的心肌细胞变得更加活跃(视频S1,支持信息)。具体而言,以C1中的心肌细胞簇为例,刺激后,心肌细胞簇两个跳动周期之间的平均停顿时间从1.382 s大大减少到0.606 s(图6e)。此外,C1中一个周期的平均收缩时间也从0.320 s减少到0.240 s(图6f)。刺激后,心肌细胞团的跳动率显着增加。图6g总结了BN-TENG的DC-EF刺激前后四个心肌细胞簇的跳动率。结果表明,在刺激后,四个簇的跳动率大大增加,尤其是对于C2和C3。 C2和C3中心肌细胞簇的跳动率增加了约8.8倍。
此外,根据统计结果,反映出刺激前后这些心肌细胞簇的分布(表S1,支持信息),刺激前变异系数为0.81,约为刺激后的2.6倍。 。这意味着在DC-EF刺激BN-TENG后,四个心肌细胞簇的跳动率变化显着降低。每个心肌细胞簇之间的跳动速率趋于更均匀,并在EF刺激后保持一致。原因可能是电刺激增强了细胞间的通讯并重新建立了功能异常的心肌细胞簇的收缩功能,这在先前的文献中得到了证实。[51–54]这种BN-TENG整合了自供电刺激该系统可直接用于协调和修复异常的心肌细胞。它可能为治疗某些心脏疾病(例如心动过缓和心律不齐)提供一种新的有效解决方案。它也潜在地用于体内重建心肌组织。
总之,我们使用五种天然材料,包括甲壳质,纤维素,SF,RP和EW,开发了具有完全生物可吸收性的BN-TENG。对这些材料的“摩擦电系列”进行了首次排名,即EW> SF>几丁质>纤维素> RP从正向负。它为使用天然材料进行的TENG设计提供了基础知识。通过修饰SF包封膜,BN-TENG在体内和体外的手术时间从几天到几周不等。分别在8至55 V的Voc和0.08至0.6μA的Isc范围内产生了多种BN-TENGs电输出。以BN-TENG为动力源,可加快功能紊乱的心肌细胞团的跳动速度,改善细胞收缩的一致性,为治疗某些心动过缓和心律不齐等心脏病提供了新的有效方法。完成其功能后,建议的BN-TENG可以在SD大鼠中完全降解和吸收。考虑到其令人印象深刻的体外和体内电输出,良好的生物相容性,可调节的生物降解性和生物吸收性,这项工作中提出的BN-TENG在未来作为瞬态电子和生物可吸收IMD的动力源具有巨大的潜力。

