最近美国癌症治疗和研究机构希望城市(City of Hope)科学家发表在著名杂志《Cell》子刊《Cell Chemical Biology》的一篇论文引起了广泛关注。它介绍了一种名为AOH1996的新型分子。该分子在肿瘤细胞中展现出独特的作用机制,对癌症细胞具有更强选择性,阻止癌细胞复制同时不影响健康细胞。当地时间8月1日,希望城市发布的新闻稿称,其科学家开发出一种口服小分子靶向化疗药物AOH1996,在临床前研究中,该研究药物能杀死所有实体瘤。

官网资料显示,希望城市成立于1913年,现已发展成为美国最大的癌症研究和治疗组织之一,该机构也是糖尿病和其他危及生命疾病的领先研究中心之一。
AOH1996这个药物的名字来自一个孩子Anna Olivia Healy,她出生于1996年,被诊断患有罕见的儿童肿瘤神经母细胞瘤后,9岁时去世。
该论文发表之后,AOH1996一时间被媒体广泛传为是“能够杀死所有实体肿瘤的抗癌神药”。事实真的如此吗?
AOH1996如何阻止癌细胞?
探讨AOH1996这一新型分子的特性和作用机制,两个关键点是转录-复制冲突(TRC)与PCNA。TRC可以理解成是细胞复制的一个关键步骤。PCNA是在TRC过程中的一个重要角色,不能没有但绝不能过多。

一、转录-复制冲突(TRC)及其导致的癌细胞基因组不稳定
转录-复制冲突(Transcription Replication Conflict, TRC)是DNA复制和RNA转录同时发生时的现象,这两个过程都需要涉及大量的蛋白质和过程。细胞复制过程中,DNA不断被转录成RNA,这是细胞后续翻译成蛋白质的关键步骤。而细胞分裂所需的复制是一个完全不同的过程,需要涉及所有DNA,复制整个基因组。因此,复制和转录两个巨大的蛋白质网络可能不时碰撞在一起,造成转录复制冲突。特别是在癌细胞中,由于其高速增殖,TRC现象更加普遍。TRC的发生可能导致DNA损伤和基因组不稳定,进而促进癌症的发生和发展。
二、AOH1996与PCNA的结合及其对TRC的干扰机制
PCNA(proliferating cell nuclear antigen)是细胞中的一个关键蛋白质,它在DNA复制和修复过程中扮演着重要角色。然而,由于复制和转录两个过程之间的冲突,PCNA可能与转录过程中的蛋白质发生竞争,导致基因组不稳定。因此,研究人员寻找一种能够干扰PCNA与转录过程的相互作用,从而抑制TRC的药物是治疗癌症的新策略之一。


AOH1996的分子结构
AOH1996是一种小分子化合物,具有特异性地与PCNA结合的能力。该化合物与PCNA的PIP盒结合腔中的特定区域结合,从而干扰PCNA与RNA聚合酶II(RPB1)的相互作用。这个干扰机制能够使RNA聚合酶II无法正常结合DNA,从而在转录依赖性情况下引起DNA双链断裂。由于癌细胞对TRC的依赖性较高,AOH1996对癌症细胞的影响比对正常细胞更具选择性。
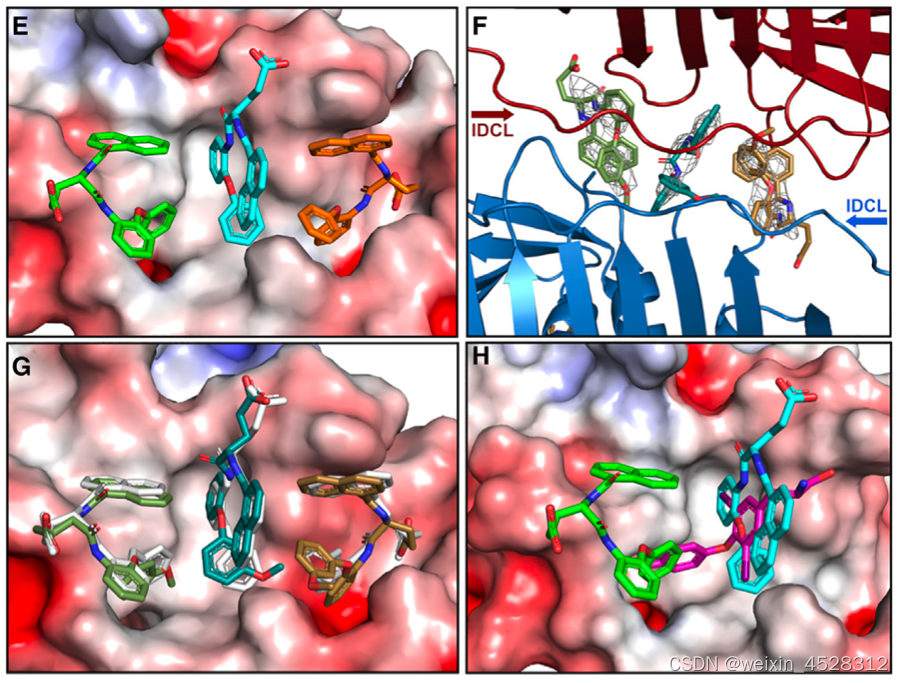 AOH1996分子和PCNA蛋白的相互作用结构解析
AOH1996分子和PCNA蛋白的相互作用结构解析
在细胞实验中,AOH1996对多种不同的癌细胞系显示出了抑制细胞生长的效果。对于70种不同的癌细胞系,50%的生长抑制所需的浓度平均约为300纳摩尔,而在多种非癌细胞系中,其毒性效应没有显现。这表明AOH1996具有潜在的治疗广谱性。

AOH1996 的药物治疗特性
动物实验到临床人体试验
一、AOH1996的动物实验结果及其临床前安全性
研究人员对AOH1996进行了动物实验,主要是在小鼠和狗等动物模型中进行了临床前毒性测试。实验结果显示,在小鼠和狗中,即使是有效剂量的6倍,AOH1996并没有出现任何明显的毒性效应。这表明AOH1996是一种安全的化合物。
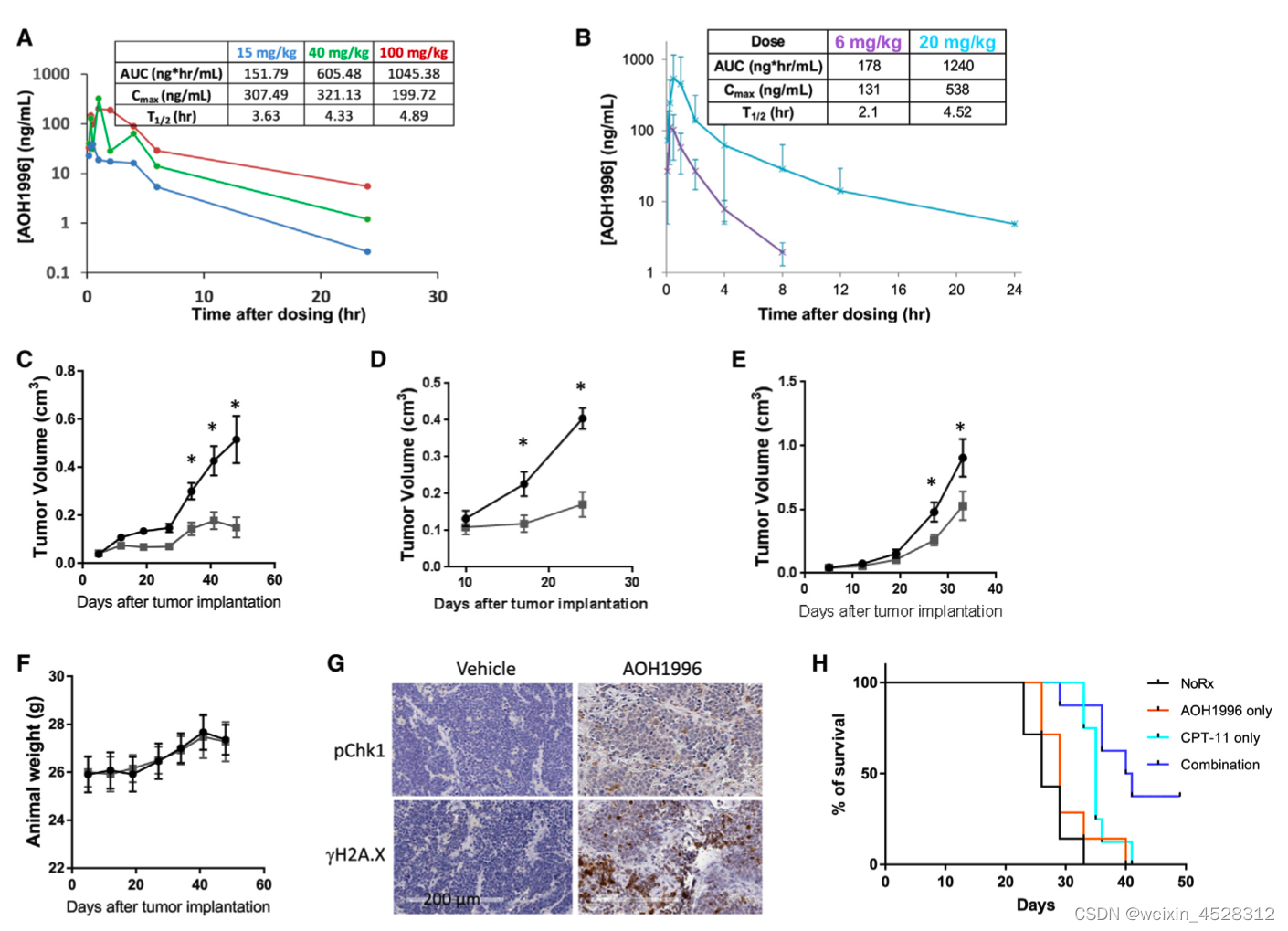
AOH1996在动物和人体体内药代动力学及抗肿瘤生长活性
二、AOH1996的临床实验进展及前景展望
为了进一步评估AOH1996的疗效和安全性,研究人员已将其推进到临床试验阶段。根据美国国家癌症研究所(NCI)的临床试验数据库(ClinicalTrials.gov),一项针对AOH1996的临床试验已于近期启动(试验编号:NCI-2021-14102)。
该临床试验将重点评估AOH1996在不同类型癌症患者中的安全性和耐受性,并进一步研究其对肿瘤的治疗效果。研究人员将招募一定数量的癌症患者,并将其分为实验组和对照组,观察并比较AOH1996在治疗中的表现。
这项临床实验在美国加州City of Hope Comprehensive Cancer Center与亚利桑那州HonorHealth Research Institute进行,该临床启动标志着AOH1996由实验室阶段迈入临床研究阶段,为其未来的临床应用提供了更加坚实的依据。如果临床试验取得积极的结果,AOH1996有望成为一种创新且有效的癌症治疗药物,为癌症患者带来新的希望和机遇。
各方专家评论
“PCNA 就像一个包含多个登机口的主要航空航站楼枢纽。数据表明PCNA在癌细胞中具有独特的改变,这一事实使我们能够设计一种仅针对癌细胞中PCNA的药物。我们的癌症杀伤药丸就像一场暴风雪,关闭了一个关键的航空枢纽,关闭了所有进出航班,只有携带癌细胞的飞机。” 论文的通讯作者、希望之城分子诊断和实验治疗学系教授Linda Malkas说。
8月3日,哈尔滨血液病肿瘤研究所马军教授在接受采访时表示,从临床来看,一款好的肿瘤药要看其有效性和安全性,目前AOH1996的研究结果来自临床前期,虽然带来了肿瘤治疗的新希望,但仍需要二三期临床试验诸多环节的证实。目前来看,肿瘤治疗没有“神药”。
“靠一个药或一个方法治愈全部癌症,目前来看还是幻想,没有神药!”马军表示,任何一种抗癌药都是从泛肿瘤研究开始,到了二三期研究才可能做单肿瘤的临床,AOH1996真正应用到临床还需要较长时间,外界需要科学严谨地看待。
马军指出,希望城市的临床前研究是针对70多个肿瘤细胞做了实验,证明有一定效果,但仅肿瘤的数量就有几百种,甚至更多。另外,目前的研究结果是来自临床前研究,还要进行二三期等确定性临床试验才能证实,因此不能认为该药可以杀死所有癌细胞。
马军进一步介绍,临床前研究和一期研究主要是看药物剂量和安全性,相关研究可发表在基础杂志上,并不代表就可以成功治疗肿瘤。CAR-T疗法也曾被称为“抗癌神药”,但全球2800个临床研究,中国占了一半,最终国产批准在临床应用的只有一种,成药极低。
“这样的论文每年没有几千,也有几百。”国内癌症科普作家李治中在其个人公众号“菠萝因子”发文表示,研究和论文本身并没有问题,只是被严重夸大和炒作了,它只是一个很正常的普通实验室肿瘤科研项目,离治病救人还有距离。
李治中提到,自己以前就是做抗癌药的临床前研究的,主要就是在实验室用各种模型来寻找和测试新型抗癌药。经常自嘲的两句话就是:我在实验室杀死了无数癌细胞,但没有缩小一个病人的肿瘤;我在实验室治愈了无数老鼠,但没有治愈一个病人。这就是临床前研究和治病救人之间的差距。
CXO巨头药明康德公众号8月3日发布的一篇文章也指出,AOH1996所展现的全面性实体瘤治疗效果仍处于细胞研究的临床前阶段,也仅在少数癌种中进行动物实验测试,而其抑制肿瘤生长的效果是否能在人体当中复制也仍是未知。即便一款药物进入1期临床试验,仍有90%的几率会以失败告终。然而随着该药物1期试验的展开,其最终是否能应用于临床上也会逐渐明朗,让我们持着客观、理性的态度拭目以待。
美国阿拉巴马大学伯明翰分校遗传学博士、新药研发从业者周叶斌指出,AOH1996距离被证实有效还差得很远。目前,该研究性药物还处于临床前实验阶段,即在体外验证药物能不能杀死癌细胞,或是在小鼠等动物模型上能不能杀死癌细胞的阶段。“这和(验证)在人身上能治疗肿瘤还差得很远。打个比方,肿瘤细胞在体外的培养皿里,我拿火烤一下,就都杀死了。但这算是发现了能杀死所有癌细胞的新疗法吗?”
此外,周叶斌认为,临床前研究中,研究人员在70多个癌症细胞系和几组正常的对照细胞中进行了测试,虽然数量很多,但远未能覆盖肿瘤的异质性。他举例,同日发表的研究中一项动物实验结果显示,AOH1996对小鼠的三种肿瘤细胞模型的抑制效果不同,其原因就在于肿瘤具有异质性,而相比实验室里的肿瘤细胞系,真实世界的肿瘤异质性更高。
周叶斌总结,这项研究展示了一种潜在新药的机理,也显示AOH1996在一些肿瘤模型中有作用。但这离真正实用还差得很远,更称不上“杀死所有实体瘤”。

论文通讯作者,Beckman Research Institute of City of Hope的Linda Malkas教授
结论
AOH1996作为一种新型分子,在干扰转录-复制冲突(TRC)对癌细胞进行选择性治疗的作用机制方面呈现出独特的优势。通过与细胞中的PCNA结合,干扰PCNA与转录机制之间的相互作用,AOH1996能够干扰转录依赖性情况下DNA复制过程,进而诱导癌细胞死亡。临床前实验数据显示,AOH1996对多种癌细胞系表现出了抑制细胞生长的效果,并且在有效剂量下对小鼠和狗等动物模型未出现明显毒性。同时,与其他化疗药物联合使用时,AOH1996还能增强其他药物的疗效,为多种癌症治疗策略提供了新的方向。
尽管如此,各方癌症治疗专家都一致地认为,应该对AOH1996的实际疗效持谨慎态度;批评媒体的报道所引起的公众期望大大超前于该项成果的实际发展。
最近一期的《Science》也发文表示,“我们希望人类癌症能够在临床上证明这种药物的功效,- 祝所有临床实验的参与者好运!”