NEWS
利用三代纳米孔测序研究m6A的
方法学进展


目前生物界中已经有超过150多种的RNA修饰碱基被报道[1],其中N6-甲基腺嘌呤(m6A)在脊椎动物中含量最为丰富,也是被研究得最为透彻的一种修饰碱基[2, 3]。目前检测m6A主要是基于二代测序的方法,这些方法存在假阳性、操作复杂以及仅限于位点检测等问题[4-11]。于是纳米孔测序技术(Oxford Nanopore Technologies,ONT)成为了一种理想的取代方法。ONT测序平台根据监测单个分子在合成聚合物膜嵌入的纳米孔中穿过时引起的电流变化直接测序DNA或RNA,修饰碱基穿孔产生的电流可能与对应的经典碱基有所不同,因此可以根据检测到的电流差异来检测包括m6A在内的修饰碱基[12,13]。自那时起,已经有十余种计算工具被开发出来(图1),用于从直接RNA测序(Direct RNA Sequencing,DRS)中鉴定m6A的位置以及确定其化学计量。
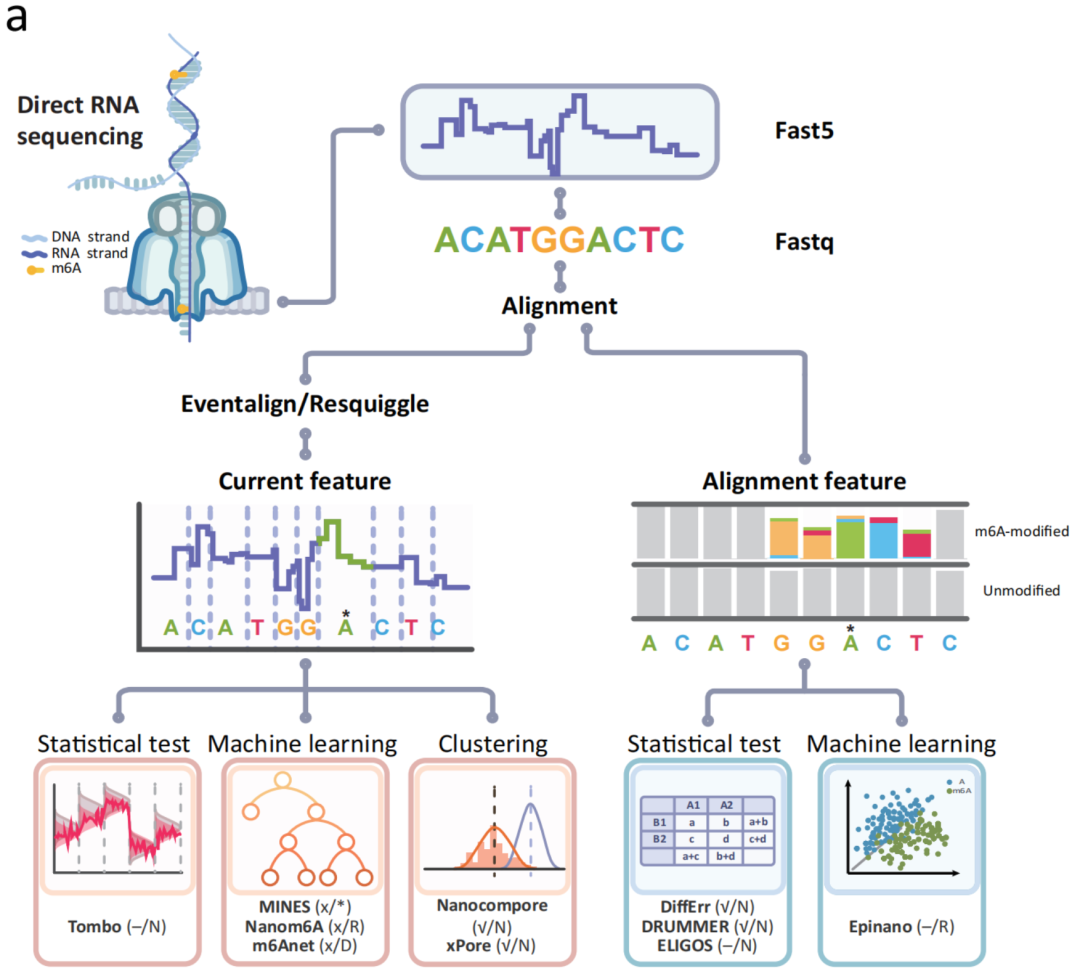
图1. 利用ONT DRS平台实现m6A检测的工具、流程以及分类
尽管已开发出许多高度复杂、先进的计算工具来检测和量化m6A,但目前仍缺乏对这些工具进行彻底评估和比较的研究。为填补这一空白,课题组于2023年4月5日在Nature Communications杂志发表论文,题为“Systematic comparison of tools used for m6A mapping from nanopore direct RNA sequencing”。
本研究利用多物种多重复(小鼠胚胎细胞和拟南芥各两个重复)样本为评估数据,以多种验证集对这些工具进行了全面评估(图2),包括使用两个连续评估指标(接受者操作特征(Receiver Operating Characteristic,ROC)和精确度-召回率(Precision Recall,PR)曲线)对它们的性能进行了定量评估,比较了它们检测出的top位点的精确度,以及它们在最优阈值下检测出的位点的准确度,召回率以及F1得分。结果发现大多数工具在精确度和召回率之间存在权衡。
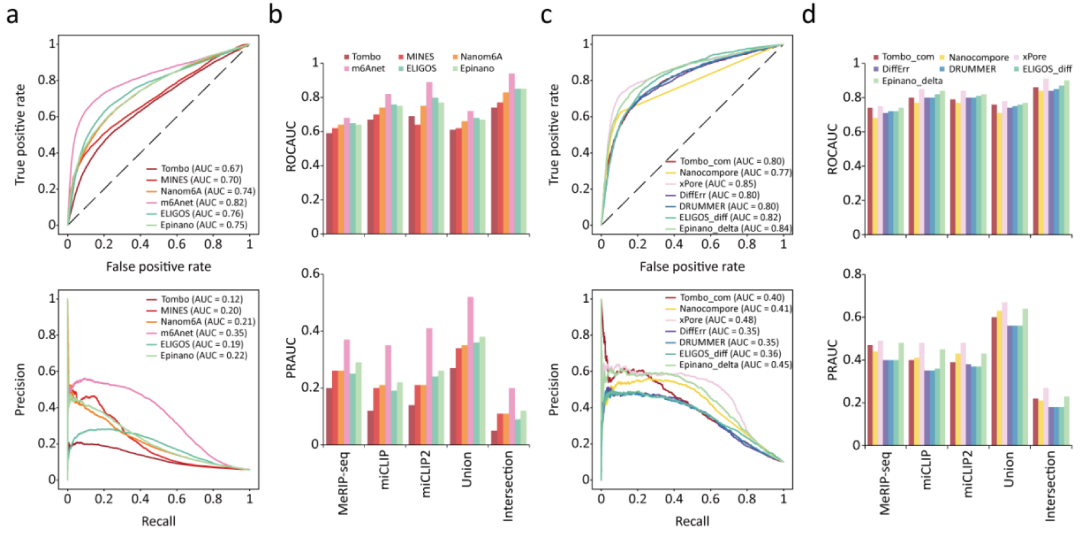
图2. 检测m6A的ONT工具能力的性能评价
除此之外,本研究还评估了这些工具在检测过程中的内在偏差,并证明引入负对照样本可以提高大多数工具的性能。此外,还发现检测能力在不同的motif之间存在差异,这是因为在某些序列上,电流差异不容易被检测到。对于可以对m6A进行定量的工具,在它们的计量估计中观察到了广泛的差异,即使在某些motif中可以获得可接受的结果。测序深度和修饰的化学计量也是另外两个重要的影响因素(图3)。
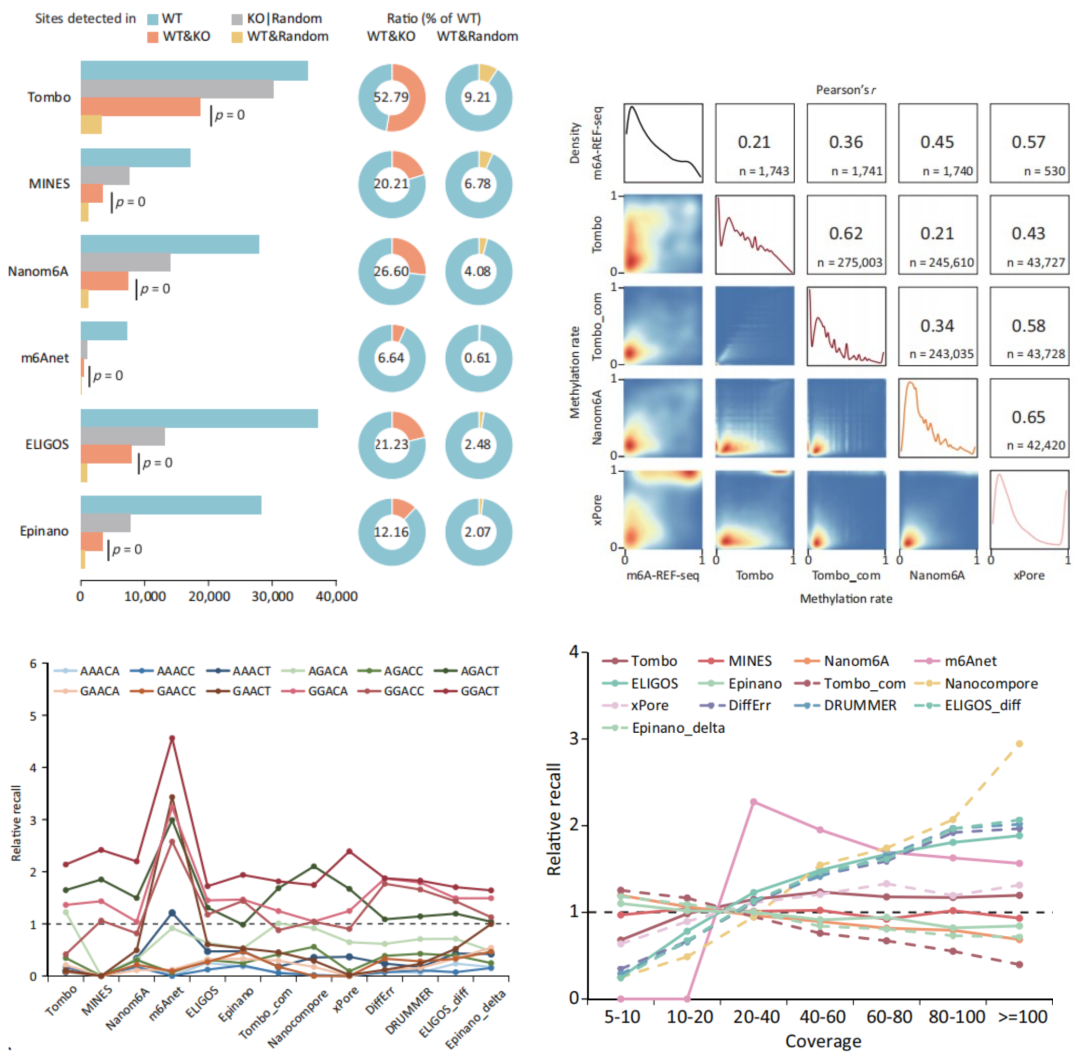
图3. 检测m6A的ONT工具的进一步分析
综上所述,研究为目前用于基于ONT DRS数据检测m6A的计算工具提供了深入的见解,并强调了进一步改进这些工具的潜力,这些可能会成为未来研究的基础。实验室成员钟振东和谢应源为文章的共同第一作者,骆观正教授和张璋副教授为通讯作者。课题组成员陈鸿萱、兰烨琳、刘学弘、纪静芸、吴赋也对该文章做出了贡献。同时还得到了广州健康院的陈捷凯研究员和香港大学Daniel W. Mak的帮助。
参考文献
1. Boccaletto, P. et al. MODOMICS: a database of RNA modification pathways. 2021 update. Nucleic Acids Res. 50, D231–D235 (2022).
2. Roundtree, I. A., Evans, M. E., Pan, T. & He, C. Dynamic RNA modifications in gene expression regulation. Cell 169, 1187–1200 (2017).
3. Zaccara, S., Ries, R. J. & Jaffrey, S. R. Reading, writing and erasing RNA methylation. Nat Rev Mol Cell Biol. 20, 608–624 (2019).
4. Meyer, K. D. et al. Comprehensive analysis of mRNA methylation reveals enrichment in 3′ UTRs and near stop codons. Cell 149, 1635–1646 (2012).
5. Dominissini, D. et al. Topology of the human and mouse m6A RNA methylomes revealed by m6A-seq. Nature 485, 201–206 (2012).
6. Garcia-Campos, M. A. et al. Deciphering the “m(6)A Code” via antibody-independent quantitative profifiling. Cell. 178, 731–747 (2019).
7. Zhang, Z. et al. Single-base mapping of m(6)A by an antibodyindependent method. Sci. Adv. 5, x250 (2019).
8. Meyer, K. D. DART-seq: an antibody-free method for global m(6)A detection. Nat. Methods 16, 1275–1280 (2019).
9. Helm, M., Lyko, F. & Motorin, Y. Limited antibody specifificity compromises epitranscriptomic analyses. Nat. Commun. 10, 5669 (2019).
10. McIntyre, A. et al. Limits in the detection of m(6)A changes using MeRIP/m(6)A-seq. Sci. Rep. 10, 6590 (2020).
11. Zhang, Z. et al. Systematic calibration of epitranscriptomic maps using a synthetic modifification-free RNA library. Nat. Methods 18, 1213–1222 (2021).
12. Simpson, J. T. et al. Detecting DNA cytosine methylation using nanopore sequencing. Nat. Methods 14, 407–410 (2017).
13. Garalde, D. R. et al. Highly parallel direct RNA sequencing on an array of nanopores. Nat. Methods 15, 201–206 (2018).

本文链接
点击页面底部“阅读原文”跳转
https://www.nature.com/articles/s41467-023-37596-5
文 / 钟
编 / 汉森萱
审 / T. Green

生物信息与表观组学
微信号|luolab2017
往期精品(点击图片直达文字对应教程)
后台回复“生信宝典福利第一波”或点击阅读原文获取教程合集