
细胞分析 | 分子图谱 | IND
生物识别 | 基因测序 | 膜蛋白
前几天,著名的结构生物科学家颜宁宣布将辞去美国普林斯顿大学教职,回国出任深圳医学科学院创始院长的消息在网上刷屏,并迅速冲上了热搜第一。
颜宁,山东章丘人,1977年11月生, 2007年受聘清华大学医学院担任教授和博士生导师,2012年获得长聘教授资格,2013年成为拜耳讲席教授。2017年受聘普林斯顿大学,成为首位雪莉·蒂尔曼终身讲席教授。
她主要致力于跨膜运输蛋白的结构与机理研究,在国际上首次揭示人源葡萄糖转运蛋白、真核生物电压门控钠离子通道和钙离子通道等一系列具有重要生理与病理意义跨膜蛋白的原子分辨率结构,为理解相关疾病的致病机理及药物开发提供了分子基础。
自2009年以来,颜宁作为通讯或者共同通讯作者发表学术研究论文近80篇,其中33篇发表于《细胞》、《自然》、《科学》。
颜宁于2005年获得Science/AAAS和GE Healthcare “青年科学家奖”(北美地区);2012年获得美国HHMI首届国际青年科学家奖、“中国优秀青年女科学家奖”;2014年获何梁何利基金科学与技术进步奖;2015年获国际蛋白质学会青年科学家奖,赛克勒国际生物物理奖,并受聘长江讲座教授(2018年终止);2016年成为戈登学术会议(Gordon Research Conference)首位来自中国大陆地区的Alexander Cruickshank报告人;2018年获亚洲及大洋洲生物化学家和分子生物学家联盟(FAOBMB)“卓越研究奖”;2019年获得以色列魏斯曼研究所颁发的国际“女科学家奖”;2021年获得国际生物物理协会颁发的Anatrace膜蛋白研究奖。

颜宁突然回国所谓何?
2014年,颜宁带领一个平均年龄不到30岁的团队,只用了6个月时间,首次解析了人源葡萄糖转运蛋白GLUT1的晶体结构和工作机理,成功攻克了横亘在全世界分子结构科学家面前长达50年的一个难题,这一成就也使得颜宁收获了无数的荣誉。而这样的研究成果并没有引发网络舆论的广泛关注。最大的两次争议,一次是离开,一次是回来。颜宁此次回国最主要的争议是:”据说她在美国已经学术破产干不下去了,因为她的工作已经被AI取代了。”很多完全不懂科学、不懂AI的键盘侠们抱着一种幸灾乐祸的感觉吃瓜。一篇网上热转的文章,开头就用极其夸张和简单的几句话概括了整个事件。
首先来看此次争议中的另一个主角——“AlphaFold”是什么?又做了什么?
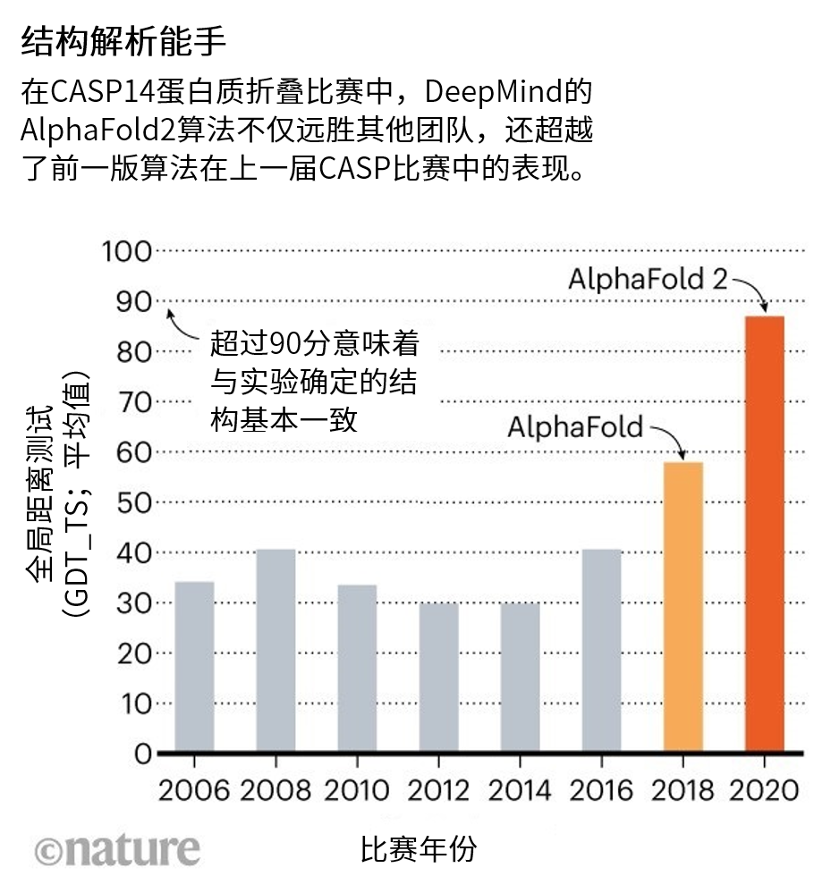
AlphaFold可以说是生物界的AlphaGo,它的所做出的贡献也被该领域的科学家们称为“划时代的进步”。同样出自于DeepMind公司AlphaFold,和横扫顶尖人类围棋职业选手的AlphaGo一样,分别在2018年(首次参加)和2020年国际蛋白质结构预测竞赛(CASP)上一举击败了其余的参会选手摘得头魁,并在生物学领域引发轰动。
在DeepMind公开了AlphaFold的源代码之后,生物学界也掀起了一阵“AlphaFold狂热”的研究。

AlphaFold诞生之前的50年中,科学家们需要进行大量的试错,耗费大量的时间和精力,采用冷冻电子显微镜、核磁共振或 X 射线晶体学等实验手段在实验室中确定蛋白质的形状。
1972年,诺贝尔化学奖得主Christian Anfinsen提出,理论上,蛋白质的氨基酸序列应该能够完全决定它的3D结构。这一假说让科学家们开始了基于氨基酸序列,通过计算方法预测蛋白质3D结构的探索。
然而,这样的探索面临着极其重大的挑战,20世纪80、90年代用计算机预测蛋白质结构的早期尝试并不成功。AlphaFold的出现改变了这一局面。2021年,DeepMind宣布已经用AlphaFold预测了人体内近乎所有蛋白质的结构,以及20个其他被大量研究的生物体的完整“蛋白质组”,其中包括小鼠和大肠杆菌,累计共有36.5万个结构。
而今年,DeepMind更是计划发布总计1亿多个结构预测——相当于所有已知蛋白的近一半,是蛋白质数据银行(PDB,Protein Data Bank)结构数据库中经过实验解析的蛋白数量的几百倍之多。颜宁的成就攻克了困扰生物学界50年的一个难题,AlphaFold的成就同样解决了困扰生物学界50年的重大挑战。
所以就有人说:你看颜宁跟她的团队研究那么久才搞出来一个结构,AlphaFold一下子就能预测出上亿个,等于是把整个游戏都颠覆了,然后像颜宁他们这样的人当然是下岗没地儿去了。
这里面有几点需要思考:
一、现在小学生都知道的无理数和虚数在历史上花费了人们上千年的思考才出现,我们不能说之前那些数学家搞得就是小学生都懂的玩意儿。
二、AI的能力来自于前人积累的数据。AlphaFold之所以能够做到这件事儿,恰恰是因为前面有科学家做了无数的理论和实验的工作,它才有一个非常好的基础。AI是站在很多个巨人的肩膀上才能达到这样的高度的,如果没有这些科学家之前的结果,AI和机器学习是不可能自己学会做生物学研究的。
三、科学家并不是只做这一件事,AI能做了他们就要被取代了。因为AlphaFold研究如此复杂,如果AI能解决的话,那恰恰是可以把这些科学家从大量重复且繁重的实验中解放出来,让他们去研究更多更有意思的课题。其实就相当于我们发明了自行车、汽车,然后它们可以帮助人类行走,这并不是意味着人类就不需要走路了,而是说人把这个时间节省下来,给人类提供了更大的自由,可以让人去做更有意义的事情。
四、颜宁并不是在国外混不下去才要回国。颜宁这样的顶级的科学家,发了这么多《Nature》、《Science》、《CELL》,仅靠闷头做做重复性的实验是不可能的。没有发过论文的人凭空臆想以为只是努力熬夜做重复工作就可以发顶刊的论文了。

深圳医学科学院为何可以吸引颜宁任职
据深圳发布报道,深圳医学科学院由市政府设立,登记为市政府举办的事业单位,实行党委领导下的院长负责制;不定编制,不定级别,实行社会化用人制度。理事会是深圳医学科学院的决策机构;院长是深圳医学科学院的法定代表人,面向全球招聘,由理事会聘任,实行任期制。
据透露,深圳医学科学院将按照全新机制的要求,主要建设“四平台一智库”,力争到本世纪中叶成为全球著名医学研究机构。
也就是说,深圳医学科学院是一所国家支持建设的全新机制医学科学院。所谓“全新机制”包括两个方面。
一、定位新
就是说,深圳医科院不仅是一个单纯的研究机构,按官方说法,它更是一个“组织科研的科研组织”。其核心功能,一要承担医学科技研究方面的公共管理和服务职能。另外,还要引领深圳医学科技发展。为此,深圳市政府还设立了“深圳市医学研究专项资金”,委托深圳医科院进行专业化管理。
二、机制新
不定编制,不定级别,自主设岗,遵循理事会治理、学术自治原则。对包括院长在内的科研人才,实行市场化薪酬、社会化用人制度。去年9月,深圳卫健委就曾发布过一波深圳医学科学院管理岗位人员的招聘。

三、政府政策的支持
机制新不止体现在人事方面。深圳医科院虽然登记为深圳市政府的直属事业单位,但本质上是一个法定机构,实行“一院一法”。具体来讲,就是政府会出台《深圳医学科学院管理办法》,可以不用顾及传统事业单位的体制,依法自主办院。
四、深圳医学科学学院财力雄厚
首先是政府专项资助,这就是上文提到的“深圳市医学研究专项资金”。今年5月份释出的文件中显示,2022年政府为其预算拨款2848万元。同时,深圳医科院还会设立联合基金、接受慈善捐赠、引入风险投资,逐步探索设立“粤港澳大湾区卫生健康科技创新引导基金”。此外,医科院的另外一大资金来源便是药物、器械的转化及生产,转化而来的收益直接反哺给自己。
五、深圳医学科学院未来发展规划
关于深圳医学科学院未来发展规划,总结下来有两点。
1)聚合资源
深圳医学科学院就相当于一个医学科技协同创新平台,解决国内医学科技资源配置分散的问题,避免资源交叉浪费,科研经费使用效率低。
2)帮助转化科研成果
深圳将允许科研人员通过“技术入股”,在转化项目中持有股份,直接参与科技成果的转化过程,提高转化积极性。
此外,深圳医科院还将通过天使投资等形式,“入股”转化企业,逐步从单一科技研发向科研产业混合体过渡。据深圳医学科学院建设方案消息,深圳医学科学院将在2025年基本建成。
颜宁也谈到:
“深圳医学科学院的一个重要使命是把研、药、医紧密结合在一起,打通从病床到实验室,再到制药公司,最后回到病床这样端到端的顺畅联系。希望深圳医学科学院不仅能够产生若干原创的科研突破,还能探索一个科学合理的机制,在保障科研人员术业有专攻,专注科研的同时,可以有效地帮助大家实现科研成果的转化。”

蓝海大脑携液冷服务器助力生命医药发展
某学院单细胞基因组研究技术中心(简称“该中心”)旨在建立标准化、自动化的工程技术,提高单细胞结构分析水平,高精度确定从蛋白质分子到全细胞的三维结构,并在此基础上揭示蛋白质及其复合体功能,大规模制备蛋白/抗体,建成具有国际一流水平和综合示范功能的蛋白质科学研究核心基地。
就生命科学研究项目而言,每个项目涉及的数据量小在上百TB。对于时间周期长、领域广的项目,未来数据需求可能在PB级。此外,该中心需要考虑支持多种生命科学研究项目,而其中,不同应用对高性能平台计算环境有不同的要求,如基因测序需要高I/O性能和内存大消耗,而分子动力学研究除了I/O性能外,还需要较高的网络和并发处理能力。
一、当前生命科学领域面临的挑战
1)数据量增长10多倍,计算能力也要“跟上”
研究团队采用的冷冻电镜技术在近两年取得了革命性的进展,具体来说就是相机技术实现了飞跃,采集数据的能力提高了10多倍,甚至上百倍,从而使得研究蛋白质结构的源数据呈几何级数增长,这就需要中心在后期全面提升数据处理和计算能力。
2)亟需简化管理保障服务品质
随着生命科学研究项目越来越多,如何根据不同项目和研究人员个性化需求分配资源,及时回收资源,实现跨整个高性能资源池的集中统一管理,简化维护管理,减轻运维人员负担,是科研高性能计算平台普遍面临问题。
3)TCO居高不下
生命科学研究迅速成为国家战略发展方向,导致研究项目和跨学科研究需求快速增加。传统的分层计算存储资源利用率低,导致新增费用快速增加。此外,能耗也成为阻碍高性能计算中心扩展的不可逾越的“高墙”。
4)网络性能不能拖后腿
作为保证高性能集群正常运行的关键,高性能网络承担着重要的连接任务。随着单节点计算和存储性能的不断提升,高性能用户需要万兆,四万兆,十万兆,InfiniBand网络选择以满足不同的高性能计算需求。

二、解决方案特点
蓝海大脑基于融合架构助力某学院单细胞基因组研究技术中心搭建了一个分布式高性能平台,拥有250个物理计算节点,5000个计算核心,总存储容量1.92PB,理论计算能力208Tflops。通过Lustre技术实现了跨20个融合架构的集中统一管理。
1)4.1TFLOPS/U的计算密度,4倍性能提升
可针对不同项目量身定制配置。其中,高密度计算节点支持14核英特尔®至强TM E5-2600v3处理器,在2U中拥有224个计算核心的密度,单U空间的计算性能密度达到业界领先的4.1TFLOPS,同时支持64个DIMM高密度内存,确保高性能和低延迟的性能要求。此外,还支持InfiniBand接口,非常适合要求超低延迟的工作负载。在强大计算能力的保证下,计算效率提升3-4倍,过去4-5天才能完成的计算任务,一天就能完成。
2)简化高性能资源池监控管理
根据项目要求定制不同的系统配置,同时通过机箱管理控制器(CMC),可以集中监控和管理20个FX系统。此外,无代理生命周期管理和一对多远程管理功能可确保BIOS和固件程序更新不会影响业务稳定性,并提高系统中计算节点生命周期管理的效率。而且在扩展服务器时,IT人员可以通过下发配置文件,使系统自动更新BIOS和固件程序,避免了重复输入配置参数的繁琐过程,减少了人工输入错误导致的系统故障,简化了管理运维,降低了管理费用。
3)TCO降低约20%
自动化、高密度、低能耗的集成部署、集中统一管理,可以使中心的TCO降低20%左右。其中,蓝海大脑将通过主板连接服务器、存储和1G0b网络,通过模块化设计形成融合一体机,同时提供散热、供电、网络、管理和PCIe扩展的共享插槽,降低数据中心的占地和能耗,帮助中心获得良好的性价比。
4)高速网络保障平台I/O性能
蓝海大脑为中心提供四万兆高性能网络,在保持成本优势的基础上,为用户提供稳定的网络性能,保证高性能、低延迟要求。
5)打破原有的服务器散热方式,采用液冷散热
蓝海大脑液冷服务器系统突破传统风冷散热模式,采用风冷和液冷混合散热模式——服务器内主要热源 CPU 利用液冷冷板进行冷却,其余热源仍采用风冷方式进行冷却。通过这种混合制冷方式,可大幅提升服务器散热效率,同时,降低主要热源 CPU 散热所耗电能,并增强服务器可靠性。经检测,采用液冷服务器配套基础设施解决方案的数据中心年均 PUE 值可降低至 1.2 以下。

三、客户收益
1)蓝海大脑HPC高性能计算与AI平台已成为高性能、多功能、专业的前沿计算平台,尤其在AI深度学习方面,为校内外生物学研究提供高效的计算支持。同时为计算生物学、深度学习、基因测序等多个研究组提供计算服务。包括测序仪的离线处理、序列搜寻比对分析、分子动力学模拟、计算机辅助药物设计和分子对接、生物网络的计算。
2)全力支持基于深度学习的分子图编码和基于深度学习的中药方剂系统的研发。研发人员可以利用HPC高性能计算和AI平台开发基于三维分子图谱的深度学习编码,进行基于深度学习的中医诊断处方。多任务分子预测模型由卷积神经网络或递归神经网络构成。交叉验证用于调整和验证参数,外部数据用于测试和评估模型。同时,从预测模型中挖掘关键信息。同时通过卷积神经网络或递归神经网络学习大量的方剂配伍信息,然后用主药生成语义自动关联分析得到的辅药,从而生成新的方剂。蓝海大脑HPC高性能计算和AI平台提供了高效并行的计算资源,大大加快了模型的训练速度,从而在有效的时间内完成最终的任务。
3)支持基于化学片段的从头计算药物设计,对疾病的治疗和生物学功能的理解有重要的促进作用。传统的药物筛选过程耗时长,成本高,导致整个药物设计和发现过程效率低下。为了加快药物设计和发现的进程,研究人员利用这一平台逐步发展了分子从头设计的方法,并取得了良好的效果。研究人员通过蒙特卡洛树搜索和神经网络模型的结合,实现了巨大化学空间的搜索和最优结构的采样,快速完成了完整的从头计算药物设计过程,并探索了蛋白质口袋表征和评分功能。
4)利用深度学习框架构建深度学习模型,加强学习模型的训练,实现深度学习的评分函数模型的训练和测试,并对模型进行训练。对于模型生成的分子,通过聚类分析分子的合成、毒性和理化性质,选择合适的分子。