目录
摘要
评估了使用 胎儿颅骨的三维参数表面模型来提取诊断性二维超声(US)图像平面
和 在胎儿生长监测中有用的生物特征测量的可行性。
参数表面变形以紧密描绘内颅边界,其拓扑保留特性定义了一个坐标空间,允许解剖区域的一致采样。

图1
从胎儿大脑中收集三个标准的轴向平面,以评估解剖完整性(图1)[1]
保留顶点之间的拓扑关系,允许创建一个胎儿颅骨的流形表示。
使用参数化表面的优点是,
从 采样颅内区域 和 在不同的表面提取平面 (不需要在图像之间进行配准)
可以识别 临床意义的关键点
由于不发达或不一致的神经解剖学标志,这在胎儿大脑图像是一个挑战。
本文测试了通过参数化平面提取标准胎儿头部平面的表面,同时保持不同受试者图像之间的解剖一致性的可行性,以及用户提供的初始表面对齐的预期准确性。
定义颅域上的标准平面

图2
标准平面是在颅表面模型(图2b)上定义的,基于它们在解剖标记的表面上应该相交的区域(图2a)。
使用单一参考脑US图像识别图像平面,每个诊断平面由欧几里得图像空间上选择三个头颅定义,Cp∈R3×3。
然后将这些点平移为定义参考图像变形表面Pj上的每个标准平面,其中j∈{TV,TT,TC},因此在颅域上。
然后对胎儿头部进行纳米等人[4]提出的表面变形过程,利用标准图像平面Pj相交的表面点U0∈NU来定义颅域的标准平面j。
图2b显示了颅骨表面标准平面的空间定义度。
实验
所有图像均被渲染为0.6mm的各向同性体素分辨率。由临床专家从3D脑容量中手动选择2D诊断平面,
平面选择验证
人工选择的(Q)和表面提取的(S)临床平面之间的二面角被计算出来作为平面之间对齐的度量。二面角,θd(Q,S),由

其中,nQ和nS分别为人工选择的平面和曲面提取的平面的法向量,并将一个向量的范数定义为

然而,需要注意的是,尽管二面角表明了平面之间的对齐,但它并不能转化为一个临床指标。更多的临床信息指标是:
a)在表面提取的平面和在人工选择的平面中可视化的感兴趣的解剖结构之间的关系,以及
b)Q平面和S平面之间的距离。例如,一个好的表面提取的TC平面会显示在手动选择的平面上可视化的小脑区域的高重叠,与手动选择的平面的平均距离(mm)很小。
解剖结构重叠是一种合适的测量方法,因为超声医生根据感兴趣的解剖结构的存在、形状和大小从三维大脑空间中选择一个合适的平面。
平面之间的重叠使用以下解剖结构的Dice系数计算:脉络膜丛(CP)、后脑室腔(聚氯乙烯)、透明隔腔(CSP)和小脑(CB)。解剖结构的骰子系数Dk是表示平面相似性的度量,由

其中,k∈{CP,聚氯乙烯,CSP,CB}和Ai (k)是结构k在平面i∈∈上出现的像素数。由于不能假定这些平面为平行的,因此预计相应的颅内结构的位置可能会发生变化。为了解释这一点,首先对强度图像进行严格配准,并对人工分割图像进行变换,然后计算骰子系数。
通过提取定义表面提取平面上颅骨轮廓的颅表面上的点,计算这些点与人工提取平面之间的平均欧氏距离,计算表面提取平面与人工选择平面之间的平均距离。颅骨轮廓点UQ定义为与表面提取平面US =(U∩S)重叠的表面点,其中U⊂NU。各点之间的欧氏距离被定义为
![]()
式中, 为单位法向量,pQ为人工提取的平面(Q)到原点的距离,点积ˆnQ·US表示表面提取平面(US)上的点在平面Q上的标量投影。
为单位法向量,pQ为人工提取的平面(Q)到原点的距离,点积ˆnQ·US表示表面提取平面(US)上的点在平面Q上的标量投影。
结果
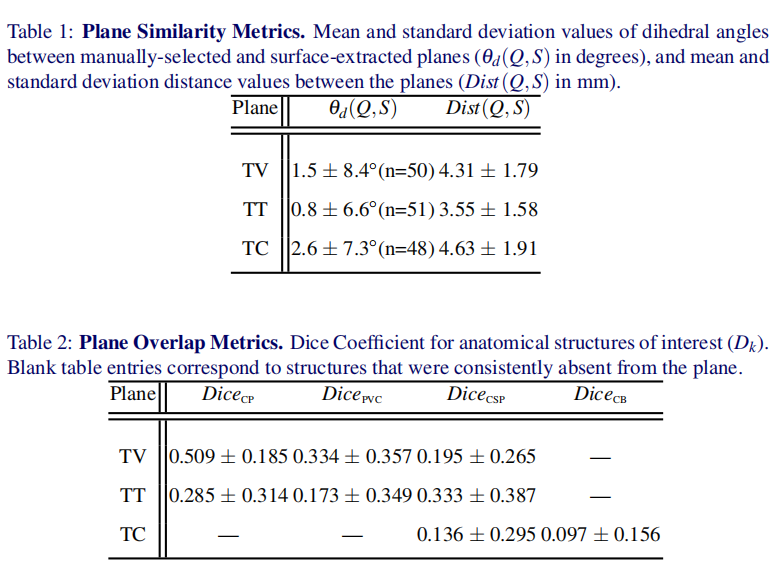
表1总结了人工选择的平面和表面提取的平面之间的二面角的平均值和标准差,
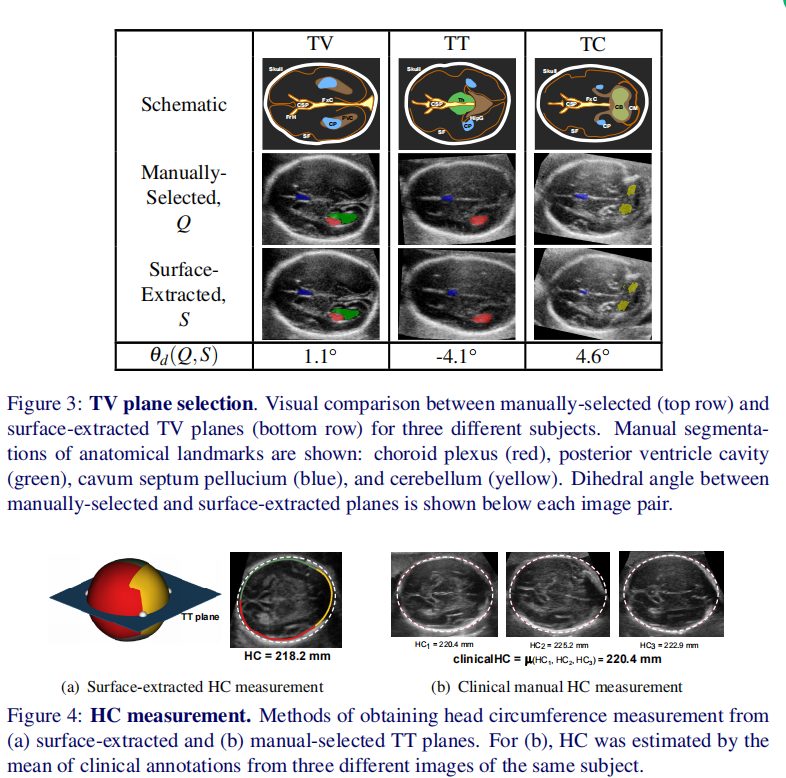
图3显示了表面提取的平面选择的可视化例子及其相应的二面角。
很明显,在所有的图像切片中,相关的解剖结构都存在在选定的平面上,无论二面角。
TT平面的Q和S平面之间的二面角最小,变量最小:
根据ISUOG指南[1],包含最多解剖标志的平面。
相比之下,由于平面的二维图像采集协议的角度和平面上预期可见的解剖标志的角度定义不精确,TC平面在平面选择上表现出最高的变异性(表2)。
表2中所列的结果排除了7.69%(4/52张图像)的被认为是异常值的图像(即|θd|≥25◦,因为图像不符合标准采集协议)。这些异常值构成了满足以下任何一个标准的图像:
临床医生选择了一个不正确的平面(由于运动伪影导致的解剖可视化不清楚),
在用户初始化过程中,颅面错位,颅内结构无法识别
所有标准平面的Q和S平面之间的平均欧氏距离均低于5mm,这表明表面提取的平面与临床医生选择的进行胎儿大脑评估的平面没有很大的偏差。
表2总结了人工选择的平面和表面提取的平面之间的分割重叠。
骰子系数值低是由于难以实现非平行Q和S平面之间的正确对齐,每个解剖结构的未定义的手工分割协议,以及每个平面上的颅内结构体积小。
然而,在每个平面上预期的结构之间存在重叠的事实表明,表面提取的平面包含了与临床医生相关的适当的颅内结构。
这突出表明,尽管一个表面提取的平面可能与临床选择的平面不完全匹配,但它仍然符合ISUOG指南[1],这意味着在胎儿神经超声评估中,它将是一个可接受的平面选择。
结果还验证了参数化表面提取不同主题的解剖一致性平面的能力。
为了评估表面提取平面的临床有效性,我们比较了从它们中收集到的头围(HC)测量值(图4a)与使用它们获得的测量值
目前最好的临床方法:从同一胎儿的不同的2D TT US扫描中收集的3个HC测量值的平均值(图4b)。两个测量之间的差异非常吻合(即RMSE=18.4mm,HC从143.4毫米到308.3毫米,18+0和我们的数据集),两种技术之间的偏差误差在HC测量的±11.1毫米,4.8%,4.8%),即低于5% [5],表明表面提取平面测量的临床可行性
结论
我们已经证明了使用胎儿颅骨的拓扑流形表示来提取诊断图像平面的可行性,从中可以提取临床有用的信息。
表面提取的平面和手动选择的平面之间的相似性依赖于用户提供表面模型和成像的大脑的精确对齐。
在本文中,我们展示了参数表面提取诊断平面的能力,该诊断平面包含一个给定平面的所有关键地标特征,尊重几何和解剖学的期望。
此外,颅表面的参数化允许在妊娠中期和晚期早期的宽胎龄窗口对不同患者的图像的解剖一致性。
最后,我们证明了从表面提取的平面获得的生物特征测量值在可接受的观察者间可变性范围内,这意味着这些平面在胎儿生长的常规评估中是可以接受的。
进一步的实验包括使用表面模型的三维性质来提取测量值,并可能应用于检测颅缝早闭或颅内[2]内的颅面畸形。