Urticaria
Referencia de cita:
Grupo de Inmunología de la Rama de Dermatología y Venereología de la Asociación Médica China: Consenso de expertos chinos sobre el diagnóstico y tratamiento de la urticaria crónica inducida (2023) [J]. Revista China de Dermatología, 2023, 56(6):479-488.doi: 10.35541/cjd.20220819
【Resumen】 La urticaria crónica inducida es un grupo de urticaria crónica inducida por desencadenantes específicos, con ronchas y/o angioedema como principales manifestaciones clínicas, y puede ir acompañada de síntomas incómodos como picazón, escozor, ardor y dolor. Las manifestaciones clínicas de esta enfermedad son muy heterogéneas, la enfermedad es prolongada y recurrente y tiene un gran impacto en la calidad de vida de los pacientes. Para mejorar la comprensión de esta enfermedad por parte de los médicos chinos y estandarizar el diagnóstico y tratamiento de la enfermedad, el Grupo de Inmunología de la Rama de Dermatología y Venereología de la Asociación Médica China basándose en los avances de la investigación clínica sobre el diagnóstico y tratamiento de la enfermedad crónica inducida. urticaria en el país y en el extranjero en los últimos años, se utilizó ampliamente el método Delphi. Se buscaron opiniones de expertos y este consenso finalmente se formó después de múltiples rondas de discusiones entre expertos relevantes.
【Palabras clave】 Urticaria; urticaria crónica inducida; signo de raspado de la piel; urticaria por contacto con el frío; urticaria colinérgica; diagnóstico; tratamiento; consenso de expertos
DOI: 10.35541/cjd.20220819
Consenso de expertos sobre diagnóstico y tratamiento de la urticaria crónica inducible en China (2023)
Grupo de Inmunología, Sociedad China de Dermatología
Autores correspondientes: Song Zhiqiang, correo electrónico: [email protected]; Gu Heng, correo electrónico: [email protected]
【Abstracto】 La urticaria crónica inducible es un grupo de urticaria crónica inducida por desencadenantes específicos, con roncha y/o angioedema como principales manifestaciones clínicas, que pueden acompañarse de picazón, hormigueo, sensación de ardor, dolor y otros síntomas desagradables. Este grupo de enfermedades se caracterizan por manifestaciones clínicas muy heterogéneas, de larga evolución y síntomas recurrentes, que tienen un gran impacto en la calidad de vida de los pacientes. Sobre la base de los avances de los estudios clínicos chinos e internacionales sobre el diagnóstico y tratamiento de la urticaria crónica inducible en los últimos años, el Grupo de Inmunología de la Sociedad China de Dermatología consultó ampliamente a expertos mediante el método Delphi y finalmente desarrolló este consenso después de varias rondas de discusión entre partes relevantes. expertos,
【Palabras clave】 Urticaria; Urticaria crónica inducible; Dermografismo sintomático; Urticaria por contacto con el frío; Urticaria colinérgica; Diagnóstico; Tratamiento; Consenso de expertos
DOI: 10.35541/cjd.20220819
La urticaria crónica se divide en urticaria crónica espontánea (UCE) y urticaria crónica inducible (CIndU). La CIndU es un grupo de urticarias inducidas por desencadenantes específicos (frío, calor, ejercicio, presión, luz solar, vibraciones, agua, etc.), siendo las principales manifestaciones clínicas las ronchas y/o angioedema. En comparación con la UCE, los factores desencadenantes de la aparición de CIndU son claros, pero su etiología es desconocida y su patogénesis es compleja. La CIndU tiene múltiples tipos y más subtipos, con manifestaciones clínicas muy heterogéneas, enfermedad prolongada y recurrente y un mayor impacto en la calidad de vida de los pacientes.
Siempre se ha prestado poca atención a esta enfermedad en China, especialmente entre los dermatólogos de base que carecen de una comprensión integral y profunda de la misma y cuyas prácticas de diagnóstico y tratamiento no están lo suficientemente estandarizadas. Actualmente, sólo la Sociedad Europea de Alergia e Inmunología Clínica en el mundo ha emitido un consenso sobre CIndU, pero no se ha actualizado en 6 años [1]. No existe una guía ni consenso de diagnóstico y tratamiento para la UCIndU en mi país. Con el fin de mejorar la comprensión de los médicos sobre CIndU y estandarizar el diagnóstico y tratamiento de CIndU, el Grupo de Inmunología de la Rama de Dermatología y Venereología de la Asociación Médica China, basándose en un resumen exhaustivo del progreso de la investigación sobre el diagnóstico y tratamiento de CIndU en el país y en el extranjero. Se consultó a expertos basándose en el método de consulta del cuestionario de expertos Delphi, y después de múltiples rondas de discusiones entre expertos relevantes, finalmente se formó este consenso [2].

1. Epidemiología
Actualmente, existen pocos estudios epidemiológicos sobre CIndU en la población china. Un estudio clínico epidemiológico multicéntrico de 2014 basado en grupos de pacientes hospitalarios de mi país mostró que la CIndU representaba el 31,9% de la urticaria crónica (de la cual la urticaria física representaba el 29,3% y la urticaria no física representaba el 2,6%). signo de raspado de la piel (también llamado urticaria artificial, 20,9%), urticaria por contacto con el frío (3,0%) y urticaria colinérgica (2,6%); en términos de distribución por género, la urticaria por contacto con el frío y la urticaria por presión retardada son más comunes en las mujeres, mientras que la urticaria colinérgica La urticaria es más común en hombres más jóvenes [3]. En términos de distribución por edades, la literatura informa que la prevalencia de CIndU en personas mayores de 65 años es menor que en personas menores de 65 años y niños menores de 14 años [4]. Una encuesta epidemiológica de 2022 basada en la población general de mi país mostró que la tasa de prevalencia de vida de CIndU fue del 1,3% [5]. Informes extranjeros indican que la prevalencia de CIndU en la población general es del 0,1% al 5,0%, y el tipo más común es consistente con las características epidemiológicas de CIndU en la población china [6].

2. Causas y patogénesis.
Al igual que en la UCE, la causa de la CIndU suele ser difícil de determinar. Los estudios han demostrado que la aparición de CIndU puede estar relacionada con la genética, antecedentes atópicos, infecciones, enfermedades del sistema sanguíneo, enfermedades autoinmunes, medicamentos, vacunas, inmunoterapia, picaduras de insectos o medusas, tatuajes, estrés mental, dieta, tracto gastrointestinal. a muchos factores, como la flora bacteriana anormal [7-13]. Por ejemplo, los pacientes con urticaria acuagénica y urticaria vibracional tienen múltiples sitios de mutación genética [7-8]; tanto la urticaria colinérgica como la urticaria por contacto por frío tienen una alta proporción de antecedentes atópicos [9, 14]; virus de la hepatitis C, VIH, Epstein-Barr virus, Toxoplasma gondii y otras infecciones pueden estar relacionadas con la aparición de urticaria de contacto por frío [14]; el bupropión y la clomipramina pueden inducir urticaria transmitida por el agua [8], y la penicilina, los anticonceptivos de acción corta, los inhibidores de la enzima convertidora de angiotensina, la griseofulvina, etc. puede inducir urticaria por contacto por frío [14], síndrome mielodisplásico, mieloma múltiple, enfermedades linfoproliferativas, linfoma de Chikin sin colesterol de células T, síndrome eosinofílico, etc., pueden estar relacionados con la aparición de urticaria por contacto por frío, urticaria por presión retardada y urticaria acuosa [8 , 14-15]; la vacuna meningocócica, la vacuna contra la hepatitis A, la vacuna neumocócica, la vacuna contra la influenza H1N1, etc. pueden inducir urticaria por contacto por frío [10].
La patogénesis exacta de CIndU no está completamente clara, pero está básicamente claro que la activación y desgranulación de los mastocitos de la piel es el vínculo central en la patogénesis de CIndU. Estudios anteriores han demostrado que existe alergia autóloga al sudor en la urticaria colinérgica [16], y que existe IgE específica de autoalérgeno en pacientes con urticaria solar [17], y que el nivel sérico total de IgE y la membrana basófila de los pacientes con CIndU Los niveles de expresión de IgE superficial son altos -receptor de afinidad (FcεRⅠ) aumentaron significativamente [18]. Esta evidencia sugiere que el mecanismo autoinmune tipo I (también conocido como autoalergia) puede ser uno de los mecanismos importantes en la patogénesis de CIndU. Se especula que varios factores físicos y no físicos Los factores estimulan al cuerpo a liberar o producir autoalérgenos, que se unen a la IgE específica de autoalérgeno en los mastocitos de la piel e inducen la reticulación, induciendo así la activación y desgranulación de los mastocitos [19]. Además, otros mecanismos diferentes también pueden estar involucrados en la patogénesis de diferentes tipos de CIndU. Por ejemplo, los mecanismos autoinmunes de tipo IIb pueden estar involucrados en la aparición de urticaria de contacto por frío y urticaria colinérgica [14, 16]; reacción de hipersensibilidad de tipo III, La activación inflamatoria sistémica y los mecanismos autoinflamatorios pueden ser más importantes para retrasar la aparición de la urticaria por presión [20]; Anomalías en la regulación de las vías neurogénicas (como los trastornos del sistema nervioso sensorial y del sistema nervioso autónomo y su inflamación neurogénica cutánea inducida) Es un mecanismo importante que no se puede ignorar en la patogénesis de la urticaria por contacto frío/calor, el angioedema por vibración, la urticaria colinérgica, la urticaria acuosa, etc. [7-8, 14, 16, 21]; los poros del sudor están bloqueados y se observa sudoración anormal (como la anhidrosis). factores clave en el desarrollo de algunos subtipos raros de urticaria colinérgica [16]; hipersensibilidad tipo I mediada por IgE específica de alérgeno exógeno y sustancias exógenas La inducción directa de la activación de los mastocitos a través de vías no inmunes son los dos mecanismos principales para la aparición del contacto urticaria [22]; los defectos en los canales iónicos, como los canales iónicos de sodio, están implicados en la aparición de urticaria acuagénica, y los canales catiónicos M-tipo-8 con potencial receptor transitorio (TRPM8) están implicados en la aparición de urticaria por contacto frío [8]. Comprender el papel de las diferentes patogénesis en la patogénesis de CIndU es útil para comprender las manifestaciones de la enfermedad y formular planes de tratamiento específicos.

3. Manifestaciones clínicas y clasificación.
La CIndU se manifiesta principalmente como ronchas y/o angioedema después de la exposición a desencadenantes, que pueden ir acompañadas de síntomas incómodos como picazón, escozor, ardor y dolor. A excepción de la urticaria por presión retardada, la mayoría de los síntomas de CIndU aparecen unos minutos después de la exposición al desencadenante. Una vez eliminado el desencadenante, los síntomas en su mayoría desaparecen por sí solos en un plazo de 0,5 a 1 hora y, por lo general, desaparecen más rápido que la UCE. Los pacientes generalmente solo presentan síntomas cutáneos y algunos pueden experimentar reacciones alérgicas graves (anafilaxia). Algunos pacientes con urticaria por presión retardada pueden experimentar síntomas sistémicos como fiebre, dolor en las articulaciones, fatiga y dolor de cabeza. La mayoría de los tipos de CIndU se pueden combinar con angioedema, entre los cuales la urticaria vibratoria, la urticaria artificial, la urticaria colinérgica y otros tipos tienen una tasa de incidencia más alta [23-24]. Pueden coexistir dos o más tipos de CIndU en un mismo paciente. Más de 1/3 de las UCE se combinan con CIndU, y el tipo más común es la urticaria artificial [25].
Según los diferentes desencadenantes, la CIndU se divide en dos categorías: urticaria física y no física. La urticaria física incluye signos de rascado de la piel, urticaria por presión retardada, urticaria de contacto por frío, urticaria de contacto térmico, urticaria solar y angioedema por vibración; la urticaria no física incluye urticaria colinérgica Sarampión, urticaria acuagénica y urticaria de contacto [26]. Cada tipo de CIndU tiene sus propias características clínicas y algunos tipos de CIndU se pueden subdividir en diferentes subtipos (consulte la Tabla 1 para obtener más detalles). El refinamiento de la clasificación clínica ayudará a un manejo preciso de la enfermedad.


4. Diagnóstico y evaluación clínica
(1) Diagnóstico de la enfermedad: el diagnóstico de CIndU se basa principalmente en el historial médico y la prueba de provocación desencadenante. El historial médico del paciente y la descripción de los síntomas son pistas diagnósticas importantes, pero los médicos deben emitir juicios objetivos sobre la información proporcionada por el paciente y evitar la fe ciega o hacer un diagnóstico basado únicamente en el historial médico y las quejas principales del paciente. El diagnóstico debe determinarse basándose en pruebas de provocación tanto como sea posible. En la actualidad, existen pruebas de provocación de desencadenante relativamente maduras para todos los tipos de CIndU, y también existen algunos equipos profesionales utilizados para la cuantificación y estandarización de las pruebas de provocación de desencadenante, como instrumentos calibrados de raspado de la piel y tableros de prueba de raspado de la piel para detectar signos de raspado de la piel (FricTest ) [27], Probador de temperatura para urticaria por contacto frío/caliente (TempTest) [28], etc. Las operaciones específicas de la prueba de provocación inducida CIndU se muestran en la Tabla 2. Cabe señalar que los antihistamínicos deben suspenderse 3 días antes de la prueba de provocación CIndU y los glucocorticoides sistémicos deben suspenderse 1 semana antes.

(2) Diagnóstico diferencial: según el historial médico del paciente y las pruebas de provocación necesarias, la mayoría de las CIndU se pueden diagnosticar con relativa claridad, pero es necesario diferenciar diferentes tipos de CIndU de otras enfermedades u otros tipos de CIndU. Ver Tabla 3.
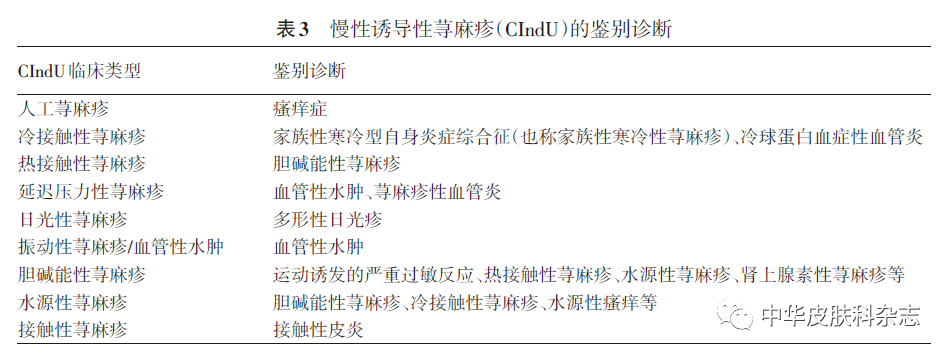
(3) Evaluación de la enfermedad: incluye principalmente el estado de la enfermedad (actividad de la enfermedad y gravedad de la enfermedad) y la evaluación de la calidad de vida del paciente. Las herramientas que se han informado para la evaluación clínica de CIndU se muestran en la Tabla 4. En vista de que las herramientas de evaluación específicas para algunos tipos de CIndU aún no se han traducido al chino, se recomienda que los médicos utilicen herramientas profesionales traducidas al chino para realizar evaluaciones clínicas periódicas de los pacientes con CIndU en función de la situación real, si es posible. , como la Escala de calificación del control de la urticaria (UCT), el Cuestionario de calidad de vida de urticaria crónica (CU-Q2oL), el Índice de calidad de vida en dermatología (DLQI), etc.

Además, la cuantificación del grado de respuesta y el umbral de estimulación de la prueba de provocación inducida de CIndU también se puede utilizar como herramienta de evaluación de la gravedad de la enfermedad. Por ejemplo, el medidor de rasguño cutáneo calibrado y FricTest pueden cuantificar el umbral de excitación de presión relativa y el grado de reacción del signo de rascado de la piel [27], TempTest puede cuantificar el umbral de excitación de temperatura de la urticaria por contacto frío/calor [28] y el mínimo Se puede confirmar el volumen de la roncha. El umbral de excitación luminosa de la urticaria solar [40], y la prueba de ejercicio controlada por pulso puede evaluar cuantitativamente el umbral de excitación del ejercicio de la urticaria colinérgica [41].
(4) Pruebas de laboratorio: cuando existe dificultad para distinguir la CIndU de otras enfermedades, o existe un alto grado de sospecha de enfermedades subyacentes subyacentes, se pueden realizar las pruebas de laboratorio pertinentes. La identificación de la urticaria por contacto por frío y la vasculitis crioglobulinémica puede mejorar las pruebas de crioglobulina, aglutinina fría, complemento, etc., y las pruebas relacionadas con el virus de la hepatitis C pueden mejorarse en pacientes con antecedentes médicos de alto riesgo. Cuando el diagnóstico diferencial de la urticaria por presión retardada es difícil, se puede completar el examen de patología de la piel. La urticaria de contacto y la dermatitis de contacto se pueden distinguir mediante una prueba de parche cutáneo (abierta). Más de la mitad de los pacientes con urticaria colinérgica tienen antecedentes atópicos, y los antecedentes atópicos de un paciente están relacionados con la gravedad de la enfermedad y la calidad de vida [9].Por lo tanto, para los pacientes con urticaria colinérgica con antecedentes claros de alergia, puede mejorar la detección de IgE alergénica e IgE total. No se recomiendan pruebas de laboratorio exhaustivas de forma rutinaria en pacientes con UCInd.

5. Tratamiento
El principio general del tratamiento de CIndU es evitar eficazmente los desencadenantes y tratar activamente los síntomas.
(1) Evitar los desencadenantes: evitar eficazmente los desencadenantes es muy importante para controlar la CIndU. Se debe guiar a los pacientes para que eviten los desencadenantes correspondientes tanto como sea posible en función de los resultados de las pruebas de provocación de desencadenantes y los umbrales correspondientes. Ver Tabla 5.

(2) Tratamiento sintomático: la mayoría de los desencadenantes son comunes en la vida diaria y los pacientes no pueden evitarlos de manera efectiva, por lo que el tratamiento sintomático es un medio importante para el manejo de la enfermedad CIndU. Según la evidencia existente basada en evidencia, el proceso de tratamiento CIndU se muestra en la Figura 1.

1. Tratamiento de primera línea: se recomiendan los antihistamínicos de segunda generación como opciones de tratamiento de primera línea para la CIndU. La última revisión sistemática muestra que los antihistamínicos de segunda generación como avastina, cetirizina, rupatadina y desloratadina tienen más evidencia acumulada en el tratamiento de la UCInd [42]. Por lo general, el medicamento se usa primero según la dosis convencional. Si el efecto no es bueno después de 1 a 2 semanas de tratamiento con la dosis convencional, se puede considerar cambiar a otras categorías, o se pueden usar dos antihistamínicos no sedantes diferentes de segunda generación. usarse juntos a la dosis convencional [43], si es necesario, se puede combinar con antihistamínicos de primera generación, o con el consentimiento informado del paciente, se puede aumentar la dosis de antihistamínicos de segunda generación de 2 a 4 veces la dosis. , y la dosis se puede reducir y mantener gradualmente después de la eficacia [44]. La respuesta al tratamiento de los diferentes tipos de CIndU a los antihistamínicos de segunda generación es bastante diferente. Entre ellos, el signo de rascado de la piel tiene la mejor respuesta al tratamiento. La anhidrosis y/o hipohidrosis, la urticaria colinérgica y el angioedema vibratorio son los mejores a los antihistamínicos de segunda generación. la respuesta al tratamiento con antihistamínicos es pobre [7,31].
2. Tratamiento de segunda línea: Para aquellos que son resistentes al tratamiento de primera línea, se recomiendan los anticuerpos monoclonales anti-IgE como opción de tratamiento de segunda línea después de una comunicación completa con el paciente. Omalizumab, un mAb IgG1κ humanizado que se une a la IgE libre, está actualmente aprobado para el tratamiento de pacientes adultos y adolescentes (a partir de 12 años) con UCE que permanecen sintomáticos a pesar del tratamiento con antihistamínicos H1. Los estudios clínicos han demostrado que omalizumab también es eficaz contra la mayoría de los tipos de CIndU [19, 45]. De acuerdo con la clasificación de evidencia y los estándares de recomendación del Centro de Medicina Basada en Evidencia de la Universidad de Oxford en el Reino Unido [46], los niveles de evidencia y recomendaciones para omalizumab en el tratamiento de diferentes tipos de UCInd se muestran en la Tabla 6. Además, sólo hay informes de casos de angioedema por vibración, lo que sugiere una mala respuesta al tratamiento con omalizumab [54], y no hay informes de urticaria de contacto al recibir tratamiento con omalizumab. El tiempo de inicio de omalizumab en el tratamiento de CIndU varía de 24 horas a 4 semanas. La respuesta al tratamiento de la urticaria artificial es la más rápida, mientras que la respuesta de la urticaria colinérgica y la urticaria de contacto por frío es más lenta y la mayoría de los pacientes mantienen La mejor tasa de respuesta es logrado a las 24 semanas de tratamiento [55]. Aún no hay una conclusión sobre cómo reducir y suspender omalizumab en el tratamiento de la UCIndU, pero este consenso recomienda que los pacientes cuyos síntomas permanezcan estables durante al menos 6 meses consideren luego reducirlo y suspenderlo gradualmente. Si los síntomas reaparecen después de la interrupción del fármaco, la reanudación del tratamiento con omalizumab sigue siendo eficaz [47].

3. Tratamiento de tercera línea: si los tratamientos anteriores no son efectivos, se puede considerar el tratamiento de tercera línea. Porque las opciones de tratamiento de tercera línea varían mucho entre los diferentes tipos de CIndU y el nivel de evidencia no es alto. Este consenso clasifica las recomendaciones para medicamentos de tratamiento de tercera línea para diversos tipos de UCInd en función de la calidad de la evidencia y la respuesta al tratamiento informada en los estudios clínicos existentes y combinada con la operabilidad clínica (Tabla 7). Entre ellos, se proporcionan algunos tipos de tratamientos de desensibilización inducida por CIndU, como terapia de desensibilización de adaptación al frío/calor, terapia de desensibilización por vibración, terapia de fotoesclerosis (desensibilización adaptativa a la luz), terapia de desensibilización por sudor autólogo, terapia de desensibilización con ejercicio o baño caliente, etc., buenos tratamientos terapéuticos. Se pueden lograr respuestas para los tipos CIndU correspondientes. Sin embargo, este tipo de tratamiento generalmente es complicado de operar, y existe cierto riesgo de inducción y exacerbación. Es difícil que los pacientes sigan el mismo durante mucho tiempo. En la práctica clínica, si se planea realizar dicho tratamiento, es necesario comunicarse plenamente con el paciente para evaluar plenamente su viabilidad, cumplimiento y beneficio general.
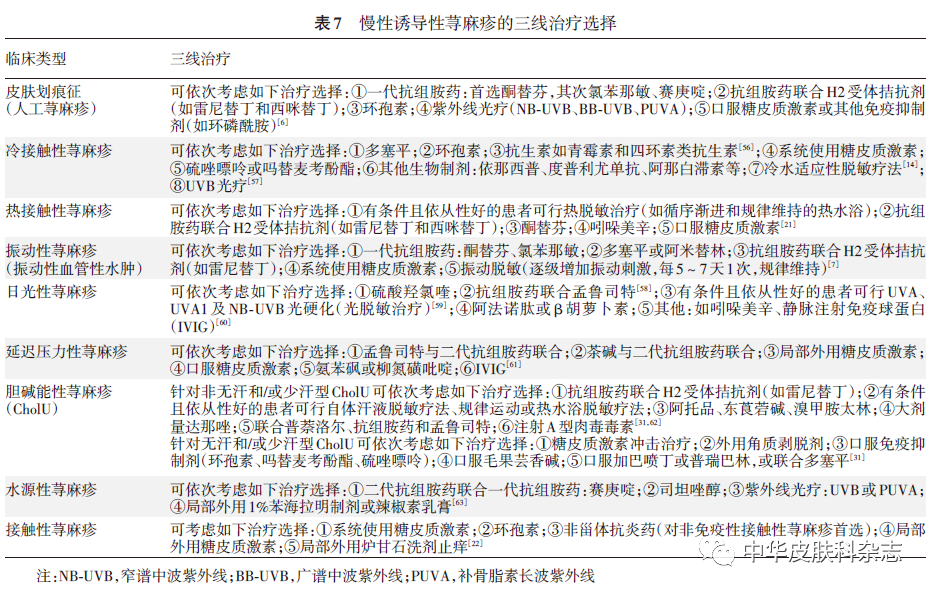
Si un pequeño número de pacientes experimenta repentinamente un agravamiento de los síntomas y signos acompañado de síntomas cardiovasculares (como palpitaciones, disminución de la presión arterial, etc.) y/o síntomas respiratorios (como dificultad para respirar, dificultad para respirar, etc.), se debe prestar atención. ante la posibilidad de reacciones alérgicas graves, y se debe administrar epinefrina y epinefrina lo antes posible./ O utilizar glucocorticoides sistémicos a corto plazo y otros tratamientos de primeros auxilios.

6. Curso natural de la enfermedad
Según informes relevantes en el extranjero, existen ciertas diferencias en el curso natural de la enfermedad entre los CIndU. Aunque la mayoría de los casos de CIndU tienen una evolución prolongada, eventualmente se recuperarán por sí solos. En general, se ha informado que la tasa de respuesta a 1 año para la urticaria física en adultos es sólo del 16,4% [64], mientras que la tasa de respuesta a 1 año para la UCInd en niños ha sido sólo del 9,6% [65]. Por lo tanto, en el proceso de gestión clínica, es necesario brindar a los pacientes educación sanitaria para que tengan suficientes expectativas psicológicas y establezcan el concepto de cooperación a largo plazo con el tratamiento y el manejo de la enfermedad. Existen ciertas diferencias en el curso natural de los diferentes tipos de CIndU (Tabla 8).


7. Declaración de consenso
Todos los expertos que participan en la formulación de este consenso declaran que se adhieren a una postura completamente objetiva, basada en el conocimiento profesional, la evidencia basada en evidencia y la experiencia clínica, siguen estrictamente el método Delphi para recopilar y ajustar opiniones, y después de una discusión completa, todos los expertos acuerdan por unanimidad formar este consenso.

8. Descargo de responsabilidad
El contenido de este consenso sólo representa las opiniones orientativas sobre el diagnóstico y tratamiento de la CIndU por parte de los expertos que participaron en su formulación, y es de referencia para los médicos. A pesar de amplias consultas y debates entre expertos, todavía existen algunas imperfecciones. El tratamiento de las enfermedades debe seguir el principio de individualización. Las sugerencias proporcionadas en este consenso no son obligatorias. Las prácticas que sean incompatibles con este consenso no significan que sean incorrectas o inapropiadas. Todavía quedan muchas preguntas por explorar en la práctica clínica, y se necesita más investigación clínica y básica para responderlas. Con el progreso continuo de la investigación clínica y básica sobre CIndU, la presentación continua de nueva evidencia basada en evidencia y la acumulación de experiencia clínica, este consenso debe revisarse y actualizarse periódicamente en el futuro para mejorar aún más el nivel de gestión de CIndU.
Relación de expertos que participaron en la formulación de este consenso (ordenados por trazos de apellido) :
Wang Gang (Hospital Xijing de la Universidad Médica de la Fuerza Aérea), Wang Fang (Primer Hospital Afiliado de la Universidad Sun Yat-sen), Wang Jianqin (Instituto de Tratamiento y Prevención Dermatológica de Guangzhou), Wang Huiping (Hospital General de la Universidad Médica de Tianjin), Yin Guangwen ( Primer Hospital Afiliado de la Universidad de Zhengzhou), Long Hai (Segundo Hospital Xiangya de la Universidad Central Sur), Sun Qing (Hospital Qilu de la Universidad de Shandong), Li Linfeng (Hospital de la Amistad de Beijing afiliado a la Universidad Médica Capital), Li Chengxin (Hospital General de la Ejército Popular de Liberación de China), Li Jie (Hospital Xiangya de la Universidad Centro Sur), Xiao Ting (Primer hospital afiliado de la Universidad Médica de China), Zou Ying (Hospital de Dermatología de Shanghai), Song Zhiqiang (Hospital Suroeste de la Universidad Médica del Ejército), Chen Qiquan (Hospital del Suroeste de la Universidad Médica del Ejército), Jin Zhehu (Hospital afiliado de la Universidad de Yanbian), Zhao Zuotao (Primer hospital de la Universidad de Pekín), Hao Fei (Tercer hospital afiliado de la Universidad médica de Chongqing), Bai Bingxue (Segundo hospital afiliado de la Universidad médica de Harbin) ), Yao Xu (Instituto de Dermatología, Academia China de Ciencias Médicas), Jin Hongzhong (Academia China de Ciencias Médicas) Peking Union Medical College Hospital), Gu Heng (Instituto de Dermatología, Academia China de Ciencias Médicas), Xu Jinhua (Huashan Hospital afiliado a la Universidad de Fudan), Xing Xinghua (El primer hospital afiliado de la Universidad Médica de China), Lu Yan (Hospital Popular Provincial de Jiangsu), Zeng Kang (Hospital Nanfang de la Universidad Médica del Sur), Xie Zhiqiang (Tercer Hospital de la Universidad de Pekín)
referencias
[1] Magerl M, Altrichter S, Borzova E, et al. La definición, las pruebas de diagnóstico y el tratamiento de las urticarias crónicas inducibles: actualización y revisión de 2016 de las recomendaciones del consenso EAACI/GA(2) LEN/EDF/UNEV[J]. Alergia, 2016,71(6):780-802. doi: 10.1111/all.12884IF: 14.710 Q1.
[2] Chen Qiquan, Yang Xianjie, Gu Heng y otros. Construyendo el "Consenso de expertos chinos sobre el diagnóstico y tratamiento de la urticaria crónica inducida (2023)" basado en el método Delphi [J]. Revista china de dermatología, 2023, 56(6):534-539.doi: 10.35541/cjd.20220814.
[3] Zhong H, Song Z, Chen W, et al. Urticaria crónica en la población china: un estudio epidemiológico multicéntrico hospitalario [J]. Alergia, 2014,69(3):359-364. doi: 10.1111/all.12338IF: 14.710 Q1.
[4] Napolitano M, Fabbrocini G, Stingeni L, et al. Prevalencia de urticaria crónica inducible en pacientes de edad avanzada [J]. J Clin Med, 2021,10(2):247. doi: 10.3390/jcm10020247IF: 4.964 Q2.
[5] Li J, Mao D, Liu S, et al. Epidemiología de la urticaria en China: un estudio poblacional [J]. Chin Med J (inglés), 2022,135(11):1369-1375. doi: 10.1097/CM9.0000000000002172IF: 6.133 Q1.
[6] Kulthanan K, Ungprasert P, Tuchinda P, et al. Dermografismo sintomático: una revisión sistemática de las opciones de tratamiento [J]. J Allergy Clin Immunol Pract, 2020,8(9):3141-3161. doi: 10. 1016/j.jaip.2020.05.016.
[7] Kulthanan K, Ungprasert P, Tapechum S, et al. Subgrupos, características y tratamiento del angioedema vibratorio: resultados de una revisión sistemática [J]. J Allergy Clin Immunol Pract, 2021,9(2):971-984. doi: 10.1016/j.jaip.2020.09.009IF: 11.022 Q1.
[8] Wang F, Zhao YK, Luo ZY, et al. Trastornos cutáneos acuagénicos[J]. J Dtsch Dermatol Ges, 2017,15(6):602-608. doi: 10.1111/ddg.13234IF: 5.231 Q1.
[9] Altrichter S, Koch K, Church MK, et al. Predisposición atópica en pacientes con urticaria colinérgica y sus implicaciones [J]. J Eur Acad Dermatol Venereol, 2016,30(12):2060-2065. doi: 10.1111/jdv.13765IF: 9.228 Q1.
[10] Raison-Peyron N, Philibert C, Bernard N, et al. Urticaria por contacto con el frío tras la vacunación: cuatro casos[J]. Acta Derm Venereol, 2016,96(6):852-853. doi: 10.2340/00015555-2358IF: 3.875 Q2.
[11] Raison-Peyron N, Litovsky J, Huet P, et al. Urticaria por contacto con el frío provocada por un tatuaje permanente[J]. J Cosmet Dermatol, 2021,20(8):2463-2465. doi: 10.1111/jocd.13874IF: 2.189 Q3.
[12] Yücel MB, Ertas R, Türk M, et al. Dermografismo sintomático dependiente de alimentos y exacerbado por alimentos: nuevas variantes del dermografismo sintomático [J]. J Allergy Clin Immunol, 2022,149(2):788-790. doi: 10.1016/j.jaci.2021.07.030IF: 14.290 Q1.
[13] Liu R, Peng C, Jing D, et al. Identificación de firmas de microbiota intestinal en dermografismo sintomático [J]. Exp Dermatol, 2021,30(12):1794-1799. doi: 10.1111/exd.14326IF: 4.511 Q1.
[14] Maltseva N, Borzova E, Fomina D, et al. Urticaria por frío: lo que sabemos y lo que no sabemos[J]. Alergia, 2021,76(4):1077-1094. doi: 10.1111/all.14674IF: 14.710 Q1.
[15] Lawlor F, Negro AK. Urticaria por presión retardada[J]. Immunol Allergy Clin North Am, 2004,24(2):247-258, vi-vii. doi: 10. 1016/j.iac.2004.01.006.
[16] Fukunaga A, Washio K, Hatakeyama M, et al. Urticaria colinérgica: epidemiología, fisiopatología, nueva categorización y manejo [J]. Clin Auton Res, 2018,28(1):103-113. doi: 10.1007/s10286-017-0418-6IF: 5.625 Q1.
[17] Lugović Mihić L, Bulat V, Situm M, et al. Reacciones cutáneas de hipersensibilidad alérgica después de la exposición al sol [J]. Coll Antropol, 2008,32 Supl 2:153-157.
[18] Giménez-Arnau AM, Ribas-Llauradó C, Mohammad-Porras N, et al. IgE and high-affinity IgE receptor in chronic inducible urticaria, pathogenic, and management relevance[J]. Clin Transl Allergy, 2022,12(2):e12117. doi: 10.1002/clt2.12117IF: 5.657 Q2 .
[19] Maurer M, Metz M, Brehler R, et al. Tratamiento con omalizumab en pacientes con urticaria crónica inducible: una revisión sistemática de la evidencia publicada [J]. J Allergy Clin Immunol, 2018,141(2):638-649. doi: 10.1016/j.jaci.2017.06.032IF: 14.290 Q1.
[20] Lenormand C, Lipsker D. Eficiencia del bloqueo de la interleucina-1 en la urticaria refractaria por presión retardada [J]. Ann Intern Med, 2012,157(8):599-600. doi: 10.7326/0003-4819-157-8-201210160-00023IF: 51.598 Q1.
[21] Pezzolo E, Peroni A, Gisondi P, et al. Urticaria por calor: una revisión de casos publicados con una actualización sobre clasificación y manejo [J]. Br J Dermatol, 2016,175(3):473-478. doi: 10.1111/bjd.14543IF: 11.113 Q1.
[22] Liu Xin, Liu Nian, Chen Hongxiang. Progresos en el diagnóstico y tratamiento de la urticaria de contacto [J]. Chinese Journal of Dermatology, 2021, 54(12):1114-1117. doi: 10.35541/cjd.20200079.
[23] Schoepke N, Młynek A, Weller K, et al. Dermografismo sintomático: una enfermedad insuficientemente descrita[J]. J Eur Acad Dermatol Venereol, 2015,29(4):708-712. doi: 10.1111/jdv.12661IF: 9.228 Q1.
[24] Mellerowicz EJ, Asady A, Maurer M, et al. El angioedema ocurre frecuentemente en la urticaria colinérgica [J]. J Allergy Clin Immunol Pract, 2019,7(4):1355-1357.e1. doi: 10.1016/j.jaip. 2018.10.013.
[25] Sánchez J, Amaya E, Acevedo A, et al. Prevalencia de urticaria inducible en pacientes con urticaria crónica espontánea: factores de riesgo asociados[J]. J Allergy Clin Immunol Pract, 2017,5(2):464-470. doi: 10.1016/j.jaip.2016.09.029IF: 11.022 Q1.
[26] Zuberbier T, Abdul Latiff AH, Abuzakouk M, et al. La guía internacional EAACI/GA2LEN/EuroGuiDerm/APAAACI para la definición, clasificación, diagnóstico y tratamiento de la urticaria[J]. Alergia, 2022,77(3):734-766. doi: 10.1111/todos. 15090.
[27] Schoepke N, Abajian M, Church MK, et al. Validación de un instrumento de provocación simplificado para el diagnóstico y prueba de umbral del dermografismo sintomático [J]. Clin Exp Dermatol, 2015,40(4):399-403. doi: 10.1111/ced.12547IF: 4.481 Q1.
[28] Magerl M, Abajian M, Krause K, et al. Un instrumento mejorado basado en el efecto Peltier para la medición del umbral de temperatura crítica en la urticaria inducida por frío y calor [J]. J Eur Acad Dermatol Venereol, 2015,29(10):2043-2045. doi: 10.1111/jdv.12739IF: 9.228 Q1.
[29] Gaebelein-Wissing N, Ellenbogen E, Lehmann P. Urticaria solar: manejo clínico, diagnóstico, curso y terapia en 27 pacientes [J]. J Dtsch Dermatol Ges, 2020,18(11):1261-1268. doi: 10.1111/ddg.14309IF: 5.231 Q1.
[30] Vergara-de-la-Campa L, Gatica-Ortega ME, Pastor-Nieto MA, et al. Urticaria-angioedema vibratorio: más conocimientos sobre los patrones de respuesta a la prueba de provocación de vórtices [J]. J Eur Acad Dermatol Venereol, 2020,34(11):e699-e701. doi: 10.1111/jdv. 16396.
[31] Fukunaga A, Oda Y, Imamura S, et al. Urticaria colinérgica: clasificación de subtipos y abordaje clínico[J]. Am J Clin Dermatol, 2022: 1-14. doi: 10.1007/s40257-022-00728-6IF: 6.233 Q1.
[32] Weller K, Groffik A, Church MK, et al. Desarrollo y validación de la prueba de control de la urticaria: un instrumento de resultados informado por el paciente para evaluar el control de la urticaria [J]. J Allergy Clin Immunol, 2014,133(5):1365-1372, 1372.e1-6. doi: 10. 1016/j.jaci.2013.12.1076.
[33] Metz M, Ohanyan T, Church MK, et al. Omalizumab es una terapia eficaz y de acción rápida en la urticaria crónica difícil de tratar: un análisis clínico retrospectivo [J]. J Dermatol Sci, 2014,73(1):57-62. doi: 10.1016/j.jdermsci.2013.08.011IF: 5.408 Q1.
[34] Baiardini I, Pasquali M, Braido F, et al. Una nueva herramienta para evaluar el impacto de la urticaria crónica en la calidad de vida: cuestionario de calidad de vida de urticaria crónica (CU-QoL) [J]. Alergia, 2005,60(8):1073-1078. doi: 10.1111/j.1398-9995.2005.00833.xIF: 14.710 Q1.
[35] Finlay AY, Khan GK. Índice de calidad de vida en dermatología (DLQI): una medida práctica sencilla para uso clínico de rutina [J]. Clin Exp Dermatol, 1994,19(3):210-216. doi: 10.1111/j.1365-2230.1994.tb01167.xIF: 4.481 Q1.
[36] Koch K, Weller K, Werner A, et al. La dosis adicional de antihistamínicos reduce la actividad de la enfermedad en pacientes con urticaria colinérgica difícil de tratar [J]. J Allergy Clin Immunol, 2016,138(5):1483-1485.e9. doi: 10.1016/j.jaci.2016.05.026IF: 14.290 Q1.
[37] Ruft J, Asady A, Staubach P, et al. Desarrollo y validación del Cuestionario de Calidad de Vida de Urticaria Colinérgica (CholU-QoL) [J]. Clin Exp Alergia, 2018,48(4):433-444. doi: 10.1111/cea.13102IF: 5.401 Q2.
[38] Młynek A, Magerl M, Siebenhaar F, et al. Resultados y relevancia de las pruebas de umbral de temperatura crítica en pacientes con urticaria adquirida por frío [J]. Br J Dermatol, 2010,162(1):198-200. doi: 10.1111/j.1365-2133.2009.09441.xIF: 11.113 Q1.
[39] Ahsan DM, Altrichter S, Gutsche A, et al. Desarrollo de la puntuación de actividad de la urticaria por frío [J]. Alergia, 2022,77(8):2509-2519. doi: 10.1111/all.15310IF: 14.710 Q1.
[40] Aguilera P. Inducción de tolerancia a la luz con terapia UV-B de banda estrecha en la urticaria solar [J]. Actas Dermosifiliogr (Ed. inglesa), 2018,109(10):853. doi: 10.1016/j.ad.2018.06.009.
[41] Altrichter S, Salow J, Ardelean E, et al. Desarrollo de una prueba ergométrica estandarizada controlada por pulso para diagnosticar e investigar la urticaria colinérgica [J]. J Dermatol Sci, 2014,75(2):88-93. doi: 10.1016/j.jdermsci.2014.04.007IF: 5.408 Q1.
[42] Dressler C, Werner RN, Eisert L, et al. Urticaria crónica inducible: una revisión sistemática de las opciones de tratamiento [J]. J Allergy Clin Immunol, 2018,141(5):1726-1734. doi: 10.1016/j.jaci.2018. 01.031.
[43] Centro de Investigación de Urticaria de la Rama de Dermatología y Venereología de la Asociación Médica China. Pautas chinas de diagnóstico y tratamiento de la urticaria (edición de 2018) [J]. Revista china de dermatología, 2019, 52(1):1-5. doi: 10.3760/cma.j.issn.0412-4030.2019.01.001.
[44] Maurer M, Fluhr JW, Khan DA. Cómo abordar la urticaria crónica inducible[J]. J Allergy Clin Immunol Pract, 2018,6(4):1119-1130. doi: 10.1016/j.jaip.2018.03.007IF: 11.022 Q1.
[45] He ZH, Qiu SC, Huang ZW, et al. Comparación entre la urticaria crónica espontánea y la urticaria crónica inducida sobre la eficacia del tratamiento con omalizumab: una revisión sistemática y un metanálisis [J]. Dermatol Ther, 2022,35(12):e15928. doi: 10.1111/dth.15928IF: 3.858 Q2.
[46] Atkins D, Best D, Briss PA, et al. Clasificación de la calidad de la evidencia y la solidez de las recomendaciones [J]. BMJ, 2004,328(7454):1490. doi: 10.1136/bmj.328.7454.1490IF: 93.333 Q1.
[47] Fialek M, Dezoteux F, Le Moing A, et al. Omalizumab en la urticaria crónica inducible: un estudio retrospectivo de la vida real [J]. Ann Dermatol Venereol, 2021,148(4):262-265. doi: 10.1016/j.ander. 2021.04.010.
[48] Maurer M, Schütz A, Weller K, et al. Omalizumab es eficaz en el dermografismo sintomático: resultados de un ensayo aleatorio controlado con placebo [J]. J Allergy Clin Immunol, 2017,140(3):870-873.e5. doi: 10.1016/j.jaci.2017.01.042IF: 14.290 Q1.
[49] Metz M, Schütz A, Weller K, et al. Omalizumab es eficaz en la urticaria por frío: resultados de un ensayo aleatorio controlado con placebo [J]. J Allergy Clin Immunol, 2017,140(3):864-867.e5. doi: 10.1016/j.jaci.2017.01.043IF: 14.290 Q1.
[50] Gastaminza G, Azofra J, Núñez-Córdoba JM, et al. Eficacia y seguridad de omalizumab (Xolair) para la urticaria colinérgica en pacientes que no responden a una dosis doble de antihistamínicos: un ensayo clínico aleatorizado, mixto, doble ciego y abierto, controlado con placebo [J]. J Allergy Clin Immunol Pract, 2019,7(5):1599-1609.e1. doi: 10.1016/j.jaip.2018.12.025IF: 11.022 Q1.
[51] Aubin F, Avenel-Audran M, Jeanmougin M, et al. Omalizumab en pacientes con urticaria solar grave y refractaria: un estudio multicéntrico de fase II [J]. J Am Acad Dermatol, 2016.74(3):574-575. doi: 10.1016/j.jaad.2015.11.021IF: 15,487 Q1.
[52] Bonnekoh H, Terhorst-Molawi D, Buttgereit T, et al. Tratamiento de la urticaria por calor grave con omalizumab: informe de un caso y revisión de la literatura[J]. J Eur Acad Dermatol Venereol, 2020,34(9):e489-e491. doi: 10.1111/jdv.16407IF: 9.228 Q1.
[53] Rorie A, Gierer S. Un caso de urticaria acuagénica tratada con éxito con omalizumab [J]. J Allergy Clin Immunol Pract, 2016,4(3):547-548. doi: 10.1016/j.jaip.2015.12.017IF: 11.022 Q1.
[54] Pressler A, Grosber M, Halle M, et al. Fracaso de omalizumab y control exitoso con ketotifeno en un paciente con angioedema vibratorio[J]. Clin Exp Dermatol, 2013,38(2):151-153. doi: 10.1111/j.1365-2230.2012.04430.xIF: 4.481 Q1.
[55] Can PK, Salman A, Hoşgören-Tekin S, et al. Efectividad de omalizumab en pacientes con urticaria crónica inducible: experiencia de la vida real en dos centros UCARE [J]. J Eur Acad Dermatol Venereol, 2021,35(10):e679-e682. doi: 10.1111/jdv.17385IF: 9.228 Q1.
[56] Gorczyza M, Schoepke N, Krause K, et al. Los pacientes con urticaria crónica por frío pueden beneficiarse del tratamiento con doxiciclina [J]. Br J Dermatol, 2017,176(1):259-261. doi: 10.1111/bjd.14820IF: 11.113 Q1.
[57] Hannuksela M, Kokkonen EL. Terapia con luz ultravioleta en la urticaria crónica [J]. Acta Derm Venereol, 1985,65(5):449-450.
[58] Levi A, Enk CD. Tratamiento de la urticaria solar mediante combinaciones de antihistamínicos y antagonistas de los receptores de leucotrienos adaptadas a la gravedad de la enfermedad [J]. Fotodermatol Photoimmunol Photomed, 2015,31(6):302-306. doi: 10.1111/phpp.12186IF: 3.254 Q2.
[59] Borzova E, Rutherford A, Konstantinou GN, et al. La fototerapia ultravioleta B de banda estrecha es beneficiosa en el dermografismo sintomático resistente a los antihistamínicos: un estudio piloto [J]. J Am Acad Dermatol, 2008,59(5):752-757. doi: 10.1016/j.jaad.2008. 07.016.
[60] Maksimovic L, Frémont G, Jeanmougin M, et al. Urticaria solar tratada con éxito con inmunoglobulinas intravenosas[J]. Dermatología, 2009,218(3):252-254. doi: 10.1159/000193998IF: 5.197 Q1.
[61] Kulthanan K, Ungprasert P, Tuchinda P, et al. Urticaria por presión retardada: una revisión sistemática de las opciones de tratamiento [J]. J Allergy Clin Immunol Pract, 2020,8(6):2035-2049.e5. doi: 10.1016/j.jaip.2020.03.004IF: 11.022 Q1.
[62] Kozaru T, Fukunaga A, Taguchi K, et al. Desensibilización rápida con sudor autólogo en la urticaria colinérgica [J]. Allergol Int, 2011,60(3):277-281. doi: 10.2332/allergolint.10-OA-0269IF: 7.478 Q1.
[63] Rujitharanawong C, Kulthanan K, Tuchinda P, et al. Una revisión sistemática de subgrupos de urticaria acuagénica y opciones de tratamiento [J]. J Allergy Clin Immunol Pract, 2022,10(8):2154-2162. doi: 10.1016/j.jaip.2022.04.033IF: 11.022 Q1.
[64] Kozel MM, Mekkes JR, Bossuyt PM, et al. Curso natural de la urticaria y angioedema físicos y crónicos en 220 pacientes[J]. J Am Acad Dermatol, 2001, 45 (3): 387-391. doi: 10.1067/mjd.2001.116217IF: 15.487 Q1.
[65] Bal F, Kahveci M, Soyer O, et al. Subtipos de urticaria crónica inducible en niños: características clínicas y pronóstico [J]. Pediatr Allergy Immunol, 2021,32(1):146-152. doi: 10.1111/pai.13324IF: 5.464 Q1.
[66] Dover JS, Black AK, Ward AM, et al. Urticaria por presión tardía. Características clínicas, investigaciones de laboratorio y respuesta al tratamiento de 44 pacientes [J]. J Am Acad Dermatol, 1988,18(6):1289-1298. doi: 10.1016/s0190-9622(88)70137-1IF: 15.487 Q1.
[67] Kim JE, Eun YS, Park YM, et al. Características clínicas de la urticaria colinérgica en Corea [J]. Ann Dermatol, 2014,26(2):189-194. doi: 10.5021/ad.2014.26.2.189IF: 0.722 T4.